
【题目】如图所示,用细线系住宽1cm的铜片使之平衡,然后在铜片一端用酒精灯加热。
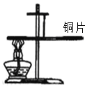
(1)加热一段时间后,发现铜片不能保持平衡,请用质量守恒定律解释其原因___________。
(2)若想用右图装置证明铜具有导热性,还需要的操作是:_____。
科目:初中化学 来源: 题型:
【题目】阅读下面短文。
酵母与泡打粉:生活中制作糕点、馒头时一般都要添加酵母或泡打粉进行发酵。在面团发酵初期,面团中的氧气和其他养分供应充足,酵母的生命活动非常旺盛,进行着有氧呼吸,淀粉水解成麦芽糖。接着面粉中原有的微量蔗糖及新产生的麦芽糖水解生成葡萄糖与果糖,最后被酵母氧化成二氧化碳和水。面团中的氧气有限,酵母的有氧呼吸逐渐转为无氧呼吸,生成的二氧化碳在面筋的网络中出不去,加热蒸烤时,二氧化碳受热膨胀,使糕点变得松软。用酵母做的食品松软可口,有特殊风味,易于消化。酵母本身含有丰富的蛋白质及维生素B,可以增加营养价值,因此面点大都用酵母发酵。糖和油对酵母菌有抑制作用。用酵母发酵耗费的时间长,而且发酵时间与温度相关(如图)。因此,也有用泡打粉来代替酵母制作糕点的。泡打粉一般是碳酸氢钠与酒石酸的混合物,通常为碳酸盐与固态酸。将泡打粉调和在面团中,碳酸氢钠与酒石酸遇水以及碳酸氢钠受热时都会产生出二氧化碳气体,使面点成为疏松、多孔的海绵状。泡打粉使用时不受发酵时间限制,随时可用,对多油多糖的面团也照样起发泡疏松的作用。缺点是它的碱性会破坏面团中的维生素,降低营养价值,若混合不均匀反而会导致面制品中有的地方碱太多发黄而不能吃。
依据文章内容回答下列问题。
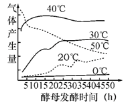
(1)用酵母和泡打粉都能使制作的面食疏松多孔,是因为_____________________________。
(2)在5-10h内,酵母发酵的最佳温度是___________。
(3)酵母本身营养丰富是因为_________________________。
(4)NaHCO3的俗称是__________________。
(5)下列有关酵母和泡打粉的说法中,正确的是___________。
A 酵母发酵的过程中既有有氧呼吸也有无氧呼吸
B 消化功能较弱的人宜食用酵母发酵制作的面食
C 泡打粉的发酵效果与面团中含糖、含油多少无关
D 酵母可以直接使面团中的淀粉转化为二氧化碳和水
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】为验证铜、铁、锌三种金属的活动性顺序,甲同学与乙同学分别设计了不同的实验方案,都能达到实验目的。实验室可供选择的试剂有:锌片、铁片、铜片、硫酸锌溶液(无色)、硫酸亚铁溶液(浅绿色)、硫酸铜溶液(蓝色),实验方案如表:
实验方案 | 方案一 | 方案二 |
实验操作 |
一种金属放入两种溶液中 |
两种金属同时放入一种溶液中 |
(1)方案一选择的金属_____;
(2)方案二中,当金属足量时,最终烧杯中液体呈_____色;
(3)其他同学设计了以下不同实验方案,其中同样可以达到实验目的有_____(填字母)
A.取一定量硫酸锌溶液,分别加入铁片与铜片
B.取一定量硫酸铜溶液,加入足量铁片充分反应后取出铁片,再加入锌片
C.取一定量硫酸亚铁溶液,加入锌片,一段时间后把锌片表面新得物质加入一定量硫酸铜溶液中
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下图所示装置用于测定空气中氧气含量,以下说法正确的是
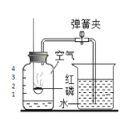
A. 使用红磷的量可多可少
B. 红磷熄灭后,立即打开止水夹
C. 整个实验过程中,集气瓶内压强持续减小
D. 最终集气瓶内的液面上升至1处,证明了空气中氧气含量
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】为探究物质溶解过程中的能量变化,某同学设计图I所示装置。在盛有水的烧杯中放入一装有饱和硝酸钾溶液的试管,向水中加入足量物质X,搅拌。结合图II硝酸钾溶解度曲线,对硝酸钾溶液变化的推断,合理的是
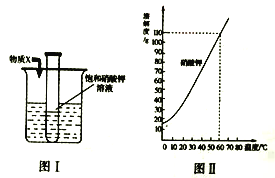
①X为NaCl固体试管中无晶体析出,硝酸钾溶液仍是饱和溶液
②X为NaOH固体,试管中无晶体析出,硝酸钾溶液仍是饱和溶液
③X为NH4NO3晶体,试管中有晶体析出,硝酸钾溶液仍是饱和溶液
④X为浓H2SO4,试管中无晶体析出,硝酸钾溶液为不饱和溶液
A. ①②③ B. ①③④ C. ①②④ D. ②③④
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】右图是 X、Y 两种微粒的结构示意图。下列说法正确的是( )

A.X 为原子,Y 为离子
B.X、Y 均属于非金属元素
C.X 在反应中可失去 6 个电子
D.X 与 Y 形成化合物的化学式为 YX
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】根据下列的实验常用仪器回答有关问题。
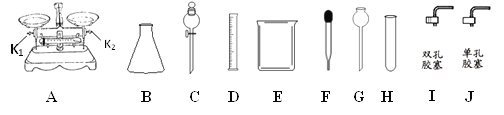
(1)仪器B的名称是__________,仪器G的名称是___________。
(2)现有一瓶溶质质量分数为35%的浓盐酸,将其稀释配制100g溶质质量分数为10%的稀盐酸,若不使用仪器A,查阅资料,必需知该浓盐酸有关________的数据,从而可以利用上述仪器中的D、E、玻璃棒和仪器_______(填序号)配制溶液。实验室制取CO2,装配一个是能够控制反应速率的发生装置,应选用上述仪器中的__________,其反应方程式为____________________________。
(3)用仪器A称量5g的NaCl固体,需要仪器A进行调平:游码归零,在两端的托盘分别放等质量的________,调节两端的平衡螺母,若天平往左端倾斜,应该将K2往_________(选填“左”或“右”,下同)调节。
(4)某微型实验装置如图,甲酸与热的浓硫酸反应生成CO ,利用CO还原氧化铁,反应过程中氧化铁的颜色变化为______。 澄清石灰水处的现象是___________,该装置为微型实验装置,微型实验的优点是__________________。
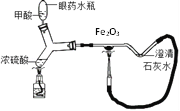
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某工厂生产的烧渣(主要含有FeO、Fe2O3和SiO2),可用于制备七水合硫酸亚铁晶体(FeSO4·7H2O),其工艺流程如下:
(资料:SiO2不溶于水,也不与稀硫酸反应。)
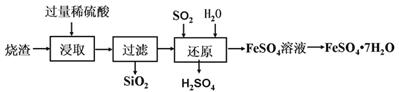
(1)“浸取”步骤中,发生反应的化学方程式有_________、Fe2O3+3H2SO4=Fe2(SO4)3+3H2O。
(2)为提高“浸取”步骤的反应速率,可采取的具体措施有_________________(写1条,不考虑“搅拌”、“使用催化剂”)
(3)“还原”的目的是将Fe3+转化为Fe2+。写出“还原”过程中反应的化学反应方程式________________。
(4)该工艺中可循环利用的物质是__________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com