
分析 首先根据题意确定物质的化学名称,然后根据题目所提供的元素、书写化学式的方法和步骤写出物质的化学式即可.
解答 解:(1)氢气燃烧的产物只有水,不会对环境造成任何污染,且热值高,是一种最理想的清洁、高效能源,故填:H2;
(2)用来中和土壤酸性的物质是氢氧化钙,化学式为:Ca(OH)2;故答案为:Ca(OH)2;
(3)赤铁矿的主要成分是氧化铁,故填:Fe2O3.
(4)氧化钙是一种氧化物,能与水反应生成氢氧化钙,是一种可用作食品干燥剂的氧化物,故填:CaO.
点评 本题主要考查学生对化学用语的书写和理解能力,题目设计既包含对化学符号意义的了解,又考查了学生对化学符号的书写,考查全面,注重基础.


科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:推断题
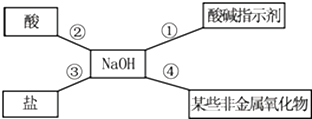
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 用如图装置模拟工业炼铁实验:
用如图装置模拟工业炼铁实验:查看答案和解析>>
科目:初中化学 来源: 题型:推断题

查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
| 实验方案 | 实验操作 | 实验现象 | 实验结论 |
| 方案一 | 取甲组反应后溶液,滴加过量碳酸钠溶液 | 有气泡产生 | 反应后硫酸溶液过量 |
| 方案二 | 取少量甲组反应后溶液,滴在pH试纸上, | 试纸变色,对比比色卡,pH<7 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
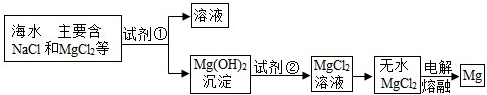
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com