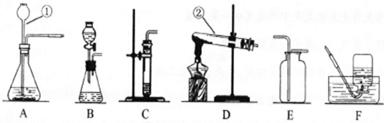
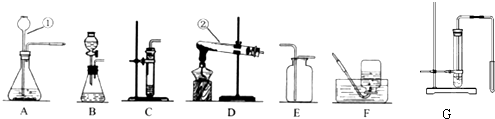
解:(1)标号仪器分别是长颈漏斗和试管是实验室常用的仪器;
(2)在常温下用石灰石和稀盐酸来制取二氧化碳,因此不需要加热.制少量二氧化碳时,可以用C装置;随时控制生产气体的量并节约药品,可用分液漏斗添加稀盐酸达到此目的,发生装置最好选用B装置;二氧化碳的密度比空气的密度大,能溶于水,因此只能用向上排空气法收集;石灰石的主要成分是碳酸钙和盐酸反应生成氯化钙、水和二氧化碳,符号表达式是:CaCO
3+2HCl=CaCl
2+H
2O+CO
2↑;二氧化碳和澄清石灰水反应生成碳酸钙沉淀和水,符号表达式是:CO
2+Ca(OH)
2═CaCO
3↓+H
2O;
(3)实验室用高锰酸钾制取氧气需要加热,属于固体加热型,故选发生装置D,高锰酸钾受热分解生成锰酸钾和二氧化锰和氧气,反应的符号表达式是:2KMnO
4
K
2MnO
4+MnO
2+O
2↑;
(4)检验O
2是否收集满的方法将带火星的木条放于集气瓶口,观察木条是否复燃进行判断;
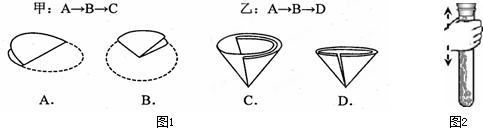
(5)导管内出现水倒流应是由于导管没先从水槽中撤出就停止了加热,致使试管内压强减小而引起水倒流;此时可再用酒精灯加热试管或把试管和导管分离,以防止水倒流入试管而引起试管炸裂,或迅速将导管移出水面或迅速将带有导管的橡皮塞取下;
故答案为:(1)长颈漏斗;试管
(2)C;E;B;CaCO
3+2HCl=CaCl
2+H
2O+CO
2↑;CO
2+Ca(OH)
2═CaCO
3↓+H
2O;
(3)D;2KMnO
4
K
2MnO
4+MnO
2+O
2↑;
(4)将带火星的木条放于集气瓶口,若木条复燃则满;
(5)继续用酒精灯加热试管;迅速将带有导管的橡皮塞取下(合理均可).
分析:(1)据常用仪器回答;
(2)据实验室制取少量二氧化碳的反应物的状态和反应条件选择发生装置,制取少量气体可选择较小的反应容器,并据二氧化碳密度、溶解性选择收集装置;分液漏斗可逐滴滴加液体,从而达到控制生成气体的量,并据反应原理书写符号表达式,二氧化碳和澄清石灰水反应生成碳酸钙沉淀和水,据此书写符号表达式;
(3)实验室用高锰酸钾制取氧气需要加热,属于固体加热型,故选发生装置D,并据反应原理书写符号表达式;
(4)检验O
2是否收集满的方法将带火星的木条放于集气瓶口,观察木条是否复燃进行判断;
(5)先熄灭了酒精灯,忘记将导管从水中取出,在水未进入导管之前,可采取的补救措施有:继续用酒精灯加热试管、迅速将导管移出水面或迅速将带有导管的橡皮塞取下.
点评:本考点主要考查了仪器的名称、气体的制取装置和收集装置的选择,同时也考查了符号表达式的书写,综合性比较强.气体的制取装置的选择与反应物的状态和反应的条件有关;气体的收集装置的选择与气体的密度和溶解性有关.


 K2MnO4+MnO2+O2↑;
K2MnO4+MnO2+O2↑; K2MnO4+MnO2+O2↑;
K2MnO4+MnO2+O2↑;