

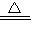 K2MnO4+MnO2+O2↑;加热时试管口放棉花的目的是防止高锰酸钾粉末进入导管,并堵塞导管;
K2MnO4+MnO2+O2↑;加热时试管口放棉花的目的是防止高锰酸钾粉末进入导管,并堵塞导管; 2H2O+O2↑;氧气的密度比空气大,可用向上排空气法收集,所以若a与c相连用排空气法来收集氧气,集气瓶要倒立,氧气不易溶于水,还可用排水法收集,气体应从短导管进入,将水挤压到集气瓶底部排尽,所以还可将瓶内装满水用排水法收集;
2H2O+O2↑;氧气的密度比空气大,可用向上排空气法收集,所以若a与c相连用排空气法来收集氧气,集气瓶要倒立,氧气不易溶于水,还可用排水法收集,气体应从短导管进入,将水挤压到集气瓶底部排尽,所以还可将瓶内装满水用排水法收集;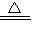 K2MnO4+MnO2+O2↑;防止高锰酸钾粉末进入导管;
K2MnO4+MnO2+O2↑;防止高锰酸钾粉末进入导管; 2H2O+O2↑;装满水或倒立.
2H2O+O2↑;装满水或倒立.

科目:初中化学 来源: 题型:
| ||
| ||
查看答案和解析>>
科目:初中化学 来源: 题型:
| ||
| △ |
| ||
| △ |
查看答案和解析>>
科目:初中化学 来源: 题型:
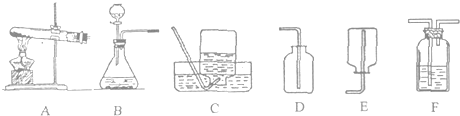
查看答案和解析>>
科目:初中化学 来源: 题型:
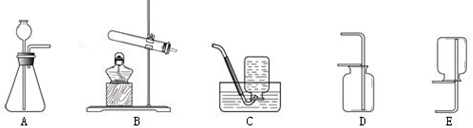
| 实验步骤 | 实验现象 | 实验结论及解释 |
| 向所取气体中加 入 |
有二氧化碳.化学方程式 为 |
查看答案和解析>>
科目:初中化学 来源: 题型:
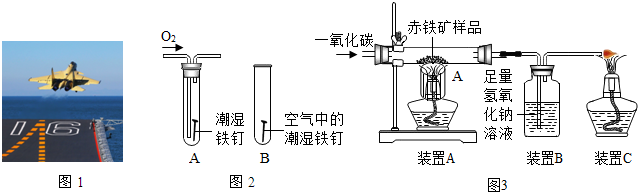
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com