
实验室有一瓶保管不当的试剂(如图),其残缺的标签中只剩下“Na”和“10%”字样。已知它是无色液体,是初中化学常用的试剂。小强和小华同学很感兴趣,决定对其成分进行探究:
【提出问题】这瓶试剂可能是什么溶液呢?
【交流讨论】根据受损标签的情况判断,这瓶试剂不可能是 。
A.酸 B.碱 C.盐
【查阅资料】
Ⅰ.初中化学常见的含钠化合物有NaCl、NaOH、Na2CO3、NaHCO3。
Ⅱ. Na2CO3和NaHCO3溶液都呈碱性。
Ⅲ.测定室温(20℃)时,四种物质的溶解度的数据如下:
| 物质 | NaCl | NaOH | Na2CO3 | NaHCO3 |
| 溶解度/g | 36 | 109 | 215 | 9.6 |
| 操作步骤 | 实验现象 | 结论及化学方程式 |
| 取样于试管中, 滴加氢氧化钙溶液 | | 猜想②正确 相关的化学方程式 |
【交流讨论】A
【得出结论】 NaHCO3
【作出猜想】NaOH
【设计并实验】(1)NaCl
(2)产生白色沉淀 Na2CO3+Ca(OH) 2=CaCO3↓+2NaOH
解析试题分析:【交流讨论】根据标签上物质的化学式是于Na开头,而酸一般是于H开头,所以这瓶试剂不可能是酸,选A
【得出结论】物质的溶解度是指在一定温度下,某固态物质在100g溶剂里达到饱和状态时所溶解的质量,用字母S表示,而饱和溶液中的溶质质量分数=S/100+S×100%,所以结合表中的溶解度数值,NaHCO3在室温(20℃)时,溶解度为9.6g,意味着此时的饱和溶液中的溶质质量分数=9.6/9.6+100×100%<10%,意思是说在室温(20℃)时,不可能配制成10%的NaHCO3溶液,故这瓶试剂不可能是NaHCO3溶液
【作出猜想】根据上面查阅的资料,再加上排除了NaHCO3,所以①可能是NaOH溶液
【设计并实验】(1)用洁净的玻璃棒蘸取该溶液滴在pH试纸上,测得pH>7,这瓶试剂不可能NaCl,因为它的水溶液呈中性,(2)检验该溶液是NaOH溶液还是Na2CO3溶液,应抓住这两者化学性质的不同点,所以取样于试管中,滴加氢氧化钙溶液,其中碳酸钠会也氢氧化钙溶液反应,生成白色沉淀碳酸钙,所以实验现象是:产生白色沉淀,发生的化学方程式:Na2CO3+Ca(OH) 2=CaCO3↓+2NaOH
考点:酸碱盐的化学性质


 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源: 题型:探究题
有一种神奇的蜡烛,点燃后任你怎么吹也吹不灭,而且看上去和普通的蜡烛一模一样,
到底是什么玄机能让蜡烛持续燃烧?请你一起参与探究。
【查阅资料】普通蜡烛由石蜡和蜡烛芯制成的,而吹不灭的蜡烛是在蜡烛芯上包裹一层打火石的粉末。打火石是由某种金属掺入少量稀土元素制成的合金,它的着火点只
有150℃。当蜡烛燃烧时,金属并不燃烧;但当蜡烛吹灭后,未冷却的金属接触到氧气就发生燃烧,从而使蜡烛复燃。
【探究与反思】这种蜡烛燃烧时,蜡烛芯里的金属为什么不燃烧? ,这种蜡烛也可以熄灭,你采用的方法是 。
【实验探究】吹不灭的蜡烛芯内的金属可能是镁、铝、铁或铜中的一种,为确定该金属的成分,请你继续探究并完成下列有关问题:(注:不考虑打火石中稀土元素对探究金属性质的影响)
| 实验 | 操作步骤 | 现象 | 结论 |
| 1 | 切开蜡烛,取出打火石,用砂纸打磨 | 打火石是银白色 | |
| 2 | | | 该金属一定不是铁 |
| 3 | 取少量打磨后的打火石于试管中,滴加硫酸铜溶液。 | 有红色物质析出 | 该金属一定是镁 |
| 操作步骤 | 现象 | 结论 |
| | | |
查看答案和解析>>
科目:初中化学 来源: 题型:探究题
(7分)化学兴趣小组用下图装置进行实验,发现镁片完全溶解、石灰水浑浊。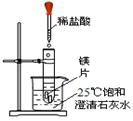
(一)石灰水变浑浊的原因是:
(1)镁和盐酸的反应 (填“吸热”或“放热”)。
(2) 。
(二)甲同学测得反应后试管内溶液pH<7
(1)该溶液呈 (填“酸”、“碱”或“中”)性。
(2)该溶液pH<7的可能原因是:
①MgCl2溶液的pH<7; ② 。
(三)乙同学将反应后试管内溶液冷却,加入镁粉并滴入酚酞,溶液颜色无变化,再加热,发现溶液慢慢浑浊且变红。
【猜想】对实验中“溶液慢慢浑浊且变红”的原因,乙同学提出猜想:
MgCl2+2H2O=Mg(OH)2↓+2HCl 大家都认为此猜想不合理,理由是 。
【查阅】资料1:Mg(OH)2难溶解于水,升高温度可加大其在水中的溶解度。
资料2:K、Ca、Na、Mg等活泼金属在一定条件下能与水反应,产生碱和气体。
【实验】丙同学在滴有酚酞的热水中加入镁粉,观察到液体慢慢变红并浑浊,镁粉表面产生气泡。收集并点燃气体,发现能燃烧,该气体是 。
用化学方程式表示:乙同学实验中“溶液慢慢浑浊且变红”的原因 。
查看答案和解析>>
科目:初中化学 来源: 题型:探究题
某化学兴趣小组的同学学习了“灭火器原理”后,设计了如图所示实验,并对反应后瓶中残留废液进行探究。
【提出问题】废液中所含溶质是什么?
【猜想与假设】
猜想1:废液中的溶质可能是NaCl、Na2CO3和HCl
猜想2:废液中的溶质只有NaCl
猜想3:废液中的溶质是NaCl和HCl
猜想4:废液中的溶质是 。
【讨论与交流】小明认为猜想1无需验证就知道是错误的,他的理由是 。
【实验与结论】
(1)为验证猜想3成立:根据盐酸性质,小王选择如图五种不同类别物质,其中X可以是 (填一种具体物质名称或化学式)。
小勇取少量于试管,滴加AgNO3溶液,产生白色沉淀,
再加稀硝酸沉淀不溶解,于是小勇认为猜想3正确,请你评价小勇的结论: 。
(2)小丽为验证猜想4成立,可选择的试剂是 。
(3)处理废液,回收利用:欲从猜想4的废液中得到纯净NaCl晶体,小芳设计了如下方案:在废液中加入适量Ca(NO3)2溶液,过滤、对滤液蒸发结晶。请评价该方案是否可行?理由 。
查看答案和解析>>
科目:初中化学 来源: 题型:探究题
(6分)某化学学习小组的同学在实验室将一定量氢氧化钙溶液与碳酸钠溶液于烧杯中充分反应。反应后溶液中的溶质是什么物质呢?大家围绕上述问题开展了下列探究活动,请你共同参与完成:
(1)氢氧化钙溶液与碳酸钠溶液反应的化学方程式为 。
(2)反应后溶液中的溶质是什么物质呢?
【猜想假设】猜想一:只有氢氧化钠
猜想二:是氢氧化钠和碳酸钠
猜想三:是 。
【实验探究】
| 实验步骤 | 实验现象 | 实验结论 |
| 步骤一:取少量溶液于试管中,滴加过量稀盐酸 | | 猜想二不正确 |
| 步骤二:取少量溶液于试管中,滴加 溶液 | 产生白色沉淀 | 猜想一不正确、猜想三正确 |
查看答案和解析>>
科目:初中化学 来源: 题型:探究题
实验室有一瓶保存不当的试剂(如右图所示),其残缺的标签中只剩下“Na”和“10%”字样。已知它是无色液体,是初中化学常用的试剂。小华等几位同学很感兴趣,决定对其成分进行探究。
【提出问题】这瓶试剂溶质是什么?
【交流研讨】根据受损标签的情况判断,这瓶试剂不可能是 (填字母序号)。
A.酸 B.碱 C.盐
【查阅资料】①初中化学常见的含钠化合物有NaCl、NaOH、Na2CO3、NaHCO3。
②Na2CO3、NaHCO3溶液都呈碱性。NaCl溶液呈中性。
③室温下(20℃)时,4种物质的溶解度的数据如下。
| 物质 | NaCl | NaOH | Na2CO3 | NaHCO3 |
| 溶解度/g | 36 | 109 | 215 | 9.6 |
| 操作步骤 | 实验现象 | 结论及化学方程式 |
| 步骤一: 取样品于试管中,滴加足量 | 产生大量的气泡 | 猜想①正确。 步骤一发生反应的化学方程式是 |
| 步骤二:把产生的气体,通入 | |
| 探究步骤 | 预计现象 | 结论 |
| 步骤一:取样品于试管中,向其中滴加足量的 溶液并过滤 | 产生白色沉淀 | 溶液中既含Na2CO3,又含有NaOH |
| 步骤二:向上述滤液中滴加酚酞试液 | 酚酞试液变 色 |
查看答案和解析>>
科目:初中化学 来源: 题型:探究题
随着人们对酒驾危害认识的加深,司法机关对于酒驾、醉驾的处罚将日趋加重。醉酒的原因是酒中含有的乙醇对人的神经系统有刺激作用。交警对呼气酒精检验的原理是:橙色的K2Cr2O7酸性溶液遇乙醇会迅速变成蓝绿色。
白酒是乙醇的水溶液,酒中的乙醇在微生物作用下能被氧化成乙酸。小刚家有一瓶密封存放的白酒,他想知道该白酒的组成情况,于是进行如下实验探究:
【提出问题】该白酒中的溶质主要有哪些?
【查阅资料】材料一:乙醇(C2H5OH),俗称酒精,易溶于水,水溶液呈中性。在加热条件下,可以把氧化铜还原为单质铜。
材料二:乙酸(CH3COOH),又名醋酸,易溶于水,具有酸的通性。
【提出猜想】猜想1:只有乙醇
猜想2:只有乙酸
猜想3:
【实验探究】
| 实验操作 | 实验现象 | 实验结论 |
| ①取少量白酒于试管中,滴入几滴橙色的K2Cr2O7酸性溶液 | | 猜想1成立 |
| ② | |
查看答案和解析>>
科目:初中化学 来源: 题型:探究题
某实验小组的同学用氢氧化钙溶液和盐酸进行酸碱中和反应的实验时,向烧杯中的氢氧化钙溶液加入稀盐酸一会后,发现忘记了滴加指示剂。因此,他们停止滴加稀盐酸,并对烧杯内溶液中的溶质成分进行探究。
Ⅰ、写出该中和反应的化学方程式: 。
Ⅱ、探究烧杯内溶液中溶质的成分。
【提出问题】该烧杯内溶液中的溶质是什么?
【猜想】猜想一:可能是CaCl2和Ca(OH)2; 猜想二:可能只有CaCl2;
猜想三: 。
【查阅资料】氯化钙溶液呈中性。
【进行实验】 实验步骤:取少量烧杯内溶液于试管中,滴入几滴酚酞溶液,振荡
实验现象: ,结论:猜想一不正确
实验步骤:实验步骤取少量烧杯内溶液于另一支试管中,逐滴加入碳酸钠溶液至过量
实验现象: 。结论:猜想二不正确,猜想三正确
【反思与拓展】
(1)在分析化学反应后所得物质成分时,除考虑生成物外还需考虑 。
(2)根据所学化学知识,验证烧杯内溶液中的溶质含有HCl,除以上方案外,下列哪些物质单独使用也能完成该实验? (填序号)
a.pH试纸 b.铜 c.紫色石蕊试液 d.硝酸银溶液
(3)烧杯中的溶液未经处理直接倒入下水道,可能造成的危害是 (写一条)。要处理烧杯内溶液,使其溶质只含有CaCl2,应向烧杯中加入过量的 。
查看答案和解析>>
科目:初中化学 来源: 题型:探究题
铁质水龙头长期使用容易生锈,小明从自家水龙头上取下一些铁锈样品,用图甲所示的装置进行实验。 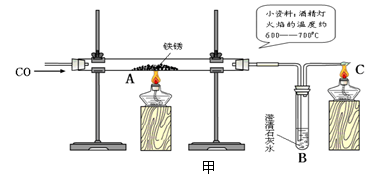
(1)B处澄清石灰水变浑浊,反应方程式为 ,C处酒精灯的作用是
(2)实验结束,小明将所得的黑色固体物质放入足量的稀硫酸中,发现没有气泡,这说明生成物中 (有或没有)铁。
为解释这个现象,小明查阅下列资料:
Ⅰ.已知铁的氧化物有FeO、Fe3O4、Fe2O3,,在一定条件下,均能逐步失去其中的氧,最终被还原为铁。
Ⅱ.某炼铁厂对氧化铁和一氧化碳进行热反应分析,获得相关数据并绘制成下图。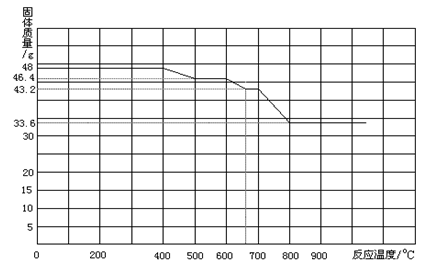
通过分析资料确定:
①700℃时氧化铁和一氧化碳进行反应的产物是 (填FeO或Fe3O4或Fe).
②小明实验失败的主要原因是 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com