
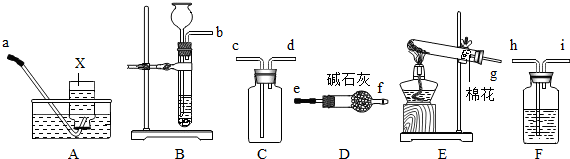
分析 (1)根据实验室常用仪器解答;
(2)根据实验室制取O2、CO2、H2的反应原理解答;
(3)根据在实验室中,通常用锌粒与稀硫酸反应来制取氢气解答;
(4)实验室常用稀盐酸和石灰石反应制取二氧化碳,要收集干燥的二氧化碳,应用浓硫酸进行干燥,二氧化碳可用向上排气法收集,据此分析回答.
(5)根据反应物的状态和反应条件,选择常用气体的发生装置;
(6)根据碳酸钙在高温的条件下生成氧化钙和二氧化碳,然后结合氧化钙的质量计算碳酸钙的质量.
解答 解:(1)根据实验室常用仪器可知:X为集气瓶;
(2)实验室制取O2可以用过氧化氢和二氧化锰,实验室制取CO2、可以用大理石和稀盐酸,实验室制取H2的可以用锌粒和稀硫酸,反应物都是固体和液体,反应条件是常温,均可选择的发生装置是B;
(3)在实验室中,通常用锌粒与稀硫酸反应来制取氢气,反应化学方程式为:Zn+H2SO4═ZnSO4+H2↑;
(4)实验室常用稀盐酸和石灰石反应制取二氧化碳,属于固液常温下反应制取气体,应选用的发生装置是B;要收集干燥的二氧化碳,应用浓硫酸进行干燥,应将气体通入到浓硫酸中,一般选用长进短出的通气方法,二氧化碳可用向上排气法收集,实验室用上述装置中选择并连接成一套组合装置,用于实验室制取干燥的CO2气体.按照气体从左至右的流向,所选装置接口的连接顺序应是:﹙b)→h→i→d→c.
(5)从题意中知道,该反应的反应物是无水醋酸钠和碱石灰的固体混合物,反应条件是加热,所以发生装置因选用E;
(6)设理论上需要碳酸钙的质量为x,
CaCO3$\frac{\underline{\;高温\;}}{\;}$CaO+CO2↑
100 56
x 5.6t
$\frac{100}{x}=\frac{56}{5.6t}$
x=10t,
含碳酸钙80%的石灰石的质量为:$\frac{10t}{80%}$=12.5t.
答案:
(1)集气瓶;
(2)B;
(3)Zn+H2SO4═ZnSO4+H2↑;
(4)﹙b)→h→i→d→c.从溶液中导出的二氧化碳气体往往含有水蒸气,要先干燥后收集;应用浓硫酸进行干燥,应将气体通入到浓硫酸中,一般选用长进短出的通气方法,二氧化碳的密度比空气的大,二氧化碳可用向上排气法收集,
(5)E;
(6)理论上需要含碳酸钙80%的石灰石的质量是12.5t
点评 明确制取氧气、二氧化碳、氢气的方法,反应原理,常用仪器,即可顺利解答,难度不大.


 夺冠训练单元期末冲刺100分系列答案
夺冠训练单元期末冲刺100分系列答案 新思维小冠军100分作业本系列答案
新思维小冠军100分作业本系列答案 名师指导一卷通系列答案
名师指导一卷通系列答案科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| 选项 | 物质 | 少量杂质 | 所加试剂和方法 |
| A | CaCl2溶液 | HCl | 过量的氢氧化钙,过滤 |
| B | H2 | 水蒸气 | 通过氢氧化钠溶液 |
| C | KCl | MnO2 | 加水溶解、过滤 |
| D | N2 | O2 | 通过灼热的铜 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
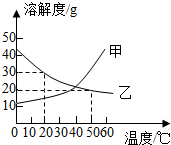 甲、乙两种固体物质的溶解度曲线如图所示,下列说法正确的是( )
甲、乙两种固体物质的溶解度曲线如图所示,下列说法正确的是( )| A. | 甲物质的溶解度大于乙物质的溶解度 | |
| B. | 甲、乙两物质的溶解度随温度升高而减小 | |
| C. | 20℃时,100g水加入20g甲可得到饱和溶液 | |
| D. | 50℃时,100g水中加入20g乙并降温至20℃,溶液由不饱和变为饱和 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A.化学之最 | B.化学与生活 |
| ①熔点最低的金属是汞 ②地壳中含量最高的金属元素是铁 ③天然存在的最硬的物质是金刚石 | ①衣服上的油污:可用汽油除去 ②水壶中的水垢:可加食盐水浸泡除去 ③冰箱中的异味:可放活性炭吸附 |
| C.物质保存方法及解释 | D.化学与工农业 |
| ①浓盐酸密封保存:防止挥发 ②白磷在冷水中保存:隔绝空气 ③氢氧化钠密封保存:防止潮解、变质 | ①用焦炭和铁矿石炼铁 ②用石油产品生产合成纤维 ③施用过量化肥,农药增加粮食产量 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
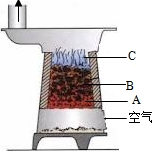 能源是人类生存和发展的基础,煤燃烧时会发生一系列化学反应.如图是北方家庭中冬天常用的煤炉,A、B、C处分别发生不同的主要反应.
能源是人类生存和发展的基础,煤燃烧时会发生一系列化学反应.如图是北方家庭中冬天常用的煤炉,A、B、C处分别发生不同的主要反应.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com