
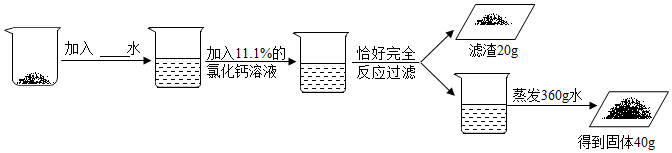
分析 (1)根据氯化钙和碳酸钠反应生成好碳酸钙沉淀和氯化钠进行分析;
(2)根据化学方程式和生成沉淀的质量进行计算;
(3)根据化学方程式计算参加反应的碳酸钠的质量和样品质量及性能计算;
(4)根据蒸发水的质量和氯化钙溶液中水的质量进行计算;
(5)根据化学方程式和样品中碳酸钠的质量分数进行计算.
解答 解:(1)氯化钙和碳酸钠反应生成好碳酸钙沉淀和氯化钠,化学方程式为:Na2CO3+CaCl2=2NaCl+CaCO3↓;
(2)设原固体中发生反应的物质的质量为x,生成氯化钠的质量为y,参加反应的氯化钙的质量为z
Na2CO3+CaCl2=2NaCl+CaCO3↓;
106 111 117 100
x z y 20g
$\frac{106}{x}$=$\frac{100}{20g}$=$\frac{117}{y}$=$\frac{111}{z}$
x=21.2g
y=23.4g
z=22.2g
(3)原固体中碳酸钠和氯化钠的质量最简整数比为21.2g:(40g-23.4g)=106:83;
(4)加入水的质量是360g-($\frac{22.2g}{11.1%}$-22.2g)=182.2g;
(5)设需样品的质量为m
Na2CO3+Ca(OH)2=2NaOH+CaCO3↓
106 80
m×$\frac{106}{106+83}$ 80kg
$\frac{106}{m×\frac{106}{106+83}}$=$\frac{80}{80kg}$
m=189kg.
故答案为:(1)Na2CO3+CaCl2=2NaCl+CaCO3↓;
(2)$\frac{106}{x}$=$\frac{100}{20g}$;
(3)106:83;
(4)182.2g;
(5)189kg.
点评 本题主要考查了化学方程式的计算,难度不大,注意解题的规范性和准确性.


 一线名师权威作业本系列答案
一线名师权威作业本系列答案科目:初中化学 来源: 题型:实验探究题



查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
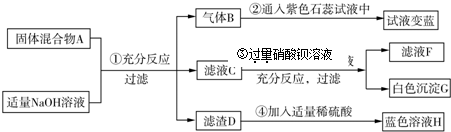
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| 选项 | A | B | C | D |
| 需区分的物质 | 软水和蒸馏水 | 氨气和二氧化碳 | 食盐水和纯碱溶液 | 聚乙烯和聚氯乙烯 |
| 方案一 | 加肥皂水搅拌 | 闻气味 | 滴加酚酞溶液 | 点燃闻气味 |
| 方案二 | 观察颜色 | 观察颜色 | 滴加食醋 | 加热,看是否熔化 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
| 实验步骤 | 实验现象 | 结论 |
| 先用pH试纸测定稀盐酸的pH,再逐渐滴加氢氧化钠溶液.并不断振荡,同时测定混合液的pH. | pH逐渐变大, 最后pH≥7 | 稀盐酸与氢氧化钠 溶液能发生反应 |
| 实验步骤 | 实验现象 | 结论 |
| 稀盐酸与氢氧化钠 溶液反应放热 |
| 实验步骤 | 实验现象 | 结论 |
| 取少量上述反应后的溶液于试管中,滴加硫酸铜溶液 | 若生成蓝色沉淀 | 氢氧化钠溶液过量 |
| 若没有明显现象 | 稀盐酸与氢氧化钠溶液恰好完全反应 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 在钢铁表面镀铬能防止钢铁生锈 | |
| B. | 浓盐酸露置于空气中质量会增大 | |
| C. | 棉纤维在空气燃烧时产生烧焦羽毛的气味 | |
| D. | 二氧化碳是造成酸雨的主要物质 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
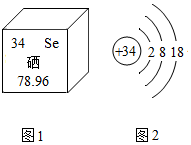 硒对人体有防癌、抗癌作用,如图1是硒元素在元素周期表中的部分信息,图2是硒元素的结构示意图,下列说法错误的是( )
硒对人体有防癌、抗癌作用,如图1是硒元素在元素周期表中的部分信息,图2是硒元素的结构示意图,下列说法错误的是( )| A. | 硒是人体必需的微量元素 | B. | 图2表示阴离子 | ||
| C. | 硒原子中子数是34 | D. | 硒是非金属元素 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | x:y=4:1 | B. | x:y=1:4 | C. | x:y=1:1 | D. | x:y=2:1 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com