
���� ��1�������������ƺ�̼������Һ���Լ��ԣ�����ʹ��̪��Һ��ɺ�ɫ��̼��������ϡ��������ɶ�����̼���������
��2����������������Һ����̼������Һ������̼��Ƴ����������
��3����Ʒ��NaOH����������������Ʒ��NaOH������������Ʒ�����������������ǿ��Ը��������غ㶨����ö�����̼�����������ݻ�ѧ����ʽ��������ȣ������Ʒ��̼���Ƶ�����������������Ʒ��NaOH���������ɽ��
��� �⣺��1��A���������ƺ�̼������Һ���Լ��ԣ�����ʹ��̪��Һ��ɺ�ɫ��B��̼��������ϡ��������ɶ�����̼���壬���������Ʋ��ܣ��ʼ�����ƿ����������Һ�Ƿ���ʵ�Ӧ�Ƿ���B��
��2���������裺ȡ��Ʒ����������������Һ��
�����а�ɫ�������ɣ�
��ѧ����ʽ��Ca��OH��2+Na2CO3=CaCO3��+2NaOH��
��3�����ɶ�����̼����Ϊ��200g+200g-395.6g=4.4g
����ȡ��Ʒ�к���Na2CO3������Ϊx��
Na2CO3+H2SO4=Na2SO4+H2O+CO2��
106 44
x 4.4g
$\frac{106}{x}=\frac{44}{4.4g}$
��ã�x=10.6g
����Ʒ��NaOH�����������ǣ�$\frac{50.0g-10.6g}{50.0g}$��100%=78.8%��
�𰸣���1����̪��Һ��ɺ�ɫ�����������ɣ� B���������ƺ�̼������Һ���Լ��ԣ�����ʹ��̪��Һ��ɺ�ɫ��
��2��ȡ��Ʒ����������������Һ���а�ɫ�������ɣ�Ca��OH��2+Na2CO3=CaCO3��+2NaOH��
��3���ռ���Ʒ��NaOH����������Ϊ78.8%��
���� ����������Ƶ�ʵ�鷽���������ۣ��Լ��Լ����ʵ�鷽������Ŀ��Ҫע�⿼�����漰���ʵĻ�ѧ���ʣ������ǵĻ�ѧ��������Ʒ������������ǽ���Ĵ���



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ̼立ֽ� | B�� | �������� | C�� | ú��ȼ�� | D�� | �ɱ����� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | һ�ֻ����� | B�� | ���ֻ����� | ||
| C�� | ���ֵ��� | D�� | һ�ֵ��ʺ�һ�ֻ�����Ļ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | Fe | B�� | CO2 | C�� | MgCI2 | D�� | HCl |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
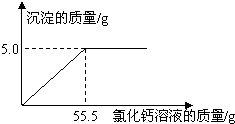 �á����������Ƽ���ƵõĴ�������������Ȼ��ƣ�Ϊ�ⶨij������Ʒ��̼���Ƶĺ�����С����ȡ�ô�����Ʒ5.5g������ܽ���44gˮ�У��ٵμ��Ȼ�����Һ����������������������Ȼ�����Һ��������ϵ����ͼ��ʾ����
�á����������Ƽ���ƵõĴ�������������Ȼ��ƣ�Ϊ�ⶨij������Ʒ��̼���Ƶĺ�����С����ȡ�ô�����Ʒ5.5g������ܽ���44gˮ�У��ٵμ��Ȼ�����Һ����������������������Ȼ�����Һ��������ϵ����ͼ��ʾ�����鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
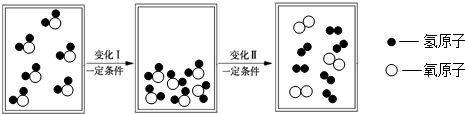
| A�� | �仯��Ϊ�����仯���仯��Ϊ��ѧ�仯 | |
| B�� | �仯��ͱ仯��ı��������Ƿ����Ƿ����˸ı� | |
| C�� | �仯��˵�����Ӽ��м���Ҽ���������¶�Ӱ�� | |
| D�� | �仯��͢���ѭ�������غ㶨�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �ø�˿��ϴˢ���ƴ��� | B�� | ̼��ƿ��������Ƽ� | ||
| C�� | ��ȼ�յķ�������������ë | D�� | �ù��IJ˵��ò����ɷ�ֹ���� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com