
分析 (1)根据铝在空气容易形成致密的氧化物,因此抗腐蚀性能很好,进行解答;
(2)根据金属有导电性,进行解答;
(3)金属铁的锈蚀条件:铁与氧气、水同时接触就会生锈;根据防止铁制品生锈(即铁锈蚀的防护)的常用措施进行解答;
(4)探究三种金属的活动性强弱顺序,根据反应的快慢和是否与酸反应.
解答 解:(1)根据铝在空气容易形成致密的氧化物,所以铝在空气中具有很好的抗腐蚀性能的原因是:铝与空气中的氧气反应,表面形成致密的氧化铝薄膜;
故答案为:铝与空气中的氧气反应,表面形成致密的氧化铝薄膜;
(2)根据金属有导电性,所以用铜制电线主要是利用铜具有良好的导电性;
故答案为:导电;
(3)金属铁的锈蚀条件:铁与氧气、水同时接触就会生锈;氧化铁和硫酸反应生成硫酸铁和水,故答案为:Fe2O3+3H2SO4═Fe2(SO4)3+3H2O;根据防止铁制品生锈的常用措施可知,防止铁制栏杆锈蚀的方法是:刷漆、涂油;
故答案为:水、氧气;刷漆、涂油;
(4)铝丝与稀硫酸反应快,推测金属活动性:铝>铁,补充铜丝插入稀硫酸中,观察是否反应,故能得出活动性Al>Fe>H>Cu的结论.
故答案为:铝丝与稀硫酸反应快;铜丝插入稀硫酸中.
点评 本题考查学生对金属的性质及金属锈蚀的条件及其防护措施的理解与在解题、生活中应用的能力.


科目:初中化学 来源: 题型:选择题
| A. | 钻木取火--摩擦生热,使可燃物的温度达到着火点而燃烧 | |
| B. | 煽风点火--使空气流通,为燃烧补充空气或氧气 | |
| C. | 釜底抽薪--取出可燃物,使燃烧更旺 | |
| D. | 百炼成钢--生铁经多次提炼,碳的含量达到钢的标准 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| 物 质 | 方法 |
| A.C(CuO) | 通入足量的CO后加热 |
| B.CaCl2溶液(HCl) | 加入过量Ca(OH)2溶液,使其充分反应 |
| C.CuSO4(H2SO4) | 加入过量CuO粉末,充分反应后过滤 |
| D.CO2(CO) | 点燃 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 能与CO2反应 | |
| B. | 只能是浓硫酸 | |
| C. | 能与水反应 | |
| D. | 能吸收空气中的水份,且不与CO2反应 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 中和反应生成盐和水,所以生成盐和水的反应一定是中和反应 | |
| B. | CO2能灭火,既利用了CO2的物理性质又利用了CO2的化学性质 | |
| C. | 碱溶液能使酚酞变红,所以能使酚酞变红的试液一定是碱溶液 | |
| D. | 酸性溶液的pH<7,所以pH<7的雨水是酸雨 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
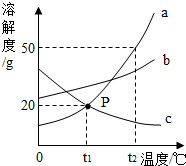 如图是a、b、c三种物质的溶解度曲线,a与c的溶解度曲线相交于P点,据图回答:
如图是a、b、c三种物质的溶解度曲线,a与c的溶解度曲线相交于P点,据图回答:查看答案和解析>>
科目:初中化学 来源: 题型:解答题
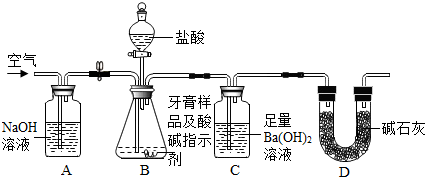
| BaCO3的质量/g | |
| 第一份 | 3.94 |
| 第二份 | 1.10 |
| 第三份 | 3.93 |
| 第四份 | 3.95 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
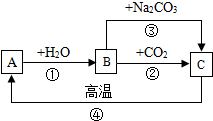 A、B、C是三种常见的含钙化合物.它们之间有如图所示的转化关系(部分产物略去):
A、B、C是三种常见的含钙化合物.它们之间有如图所示的转化关系(部分产物略去):查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com