
| A. |  | B. | 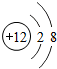 | C. | 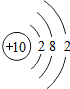 | D. |  |
 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | -2 | B. | +2 | C. | +4 | D. | +6 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | Y>X>Z | B. | X>Y>Z | C. | Y>Z>X | D. | Z>Y>X |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
 现有甲、乙、丙三种金属,采用将其中的一种金属分别放入另外两种金属的硫酸盐溶液中的方法进行实验,得到三种金属间的转化关系(如图所示),则三种金属活动性由强到弱的顺序是( )
现有甲、乙、丙三种金属,采用将其中的一种金属分别放入另外两种金属的硫酸盐溶液中的方法进行实验,得到三种金属间的转化关系(如图所示),则三种金属活动性由强到弱的顺序是( )| A. | 乙、甲、丙 | B. | 乙、丙、甲 | C. | 丙、甲、乙 | D. | 丙、乙、甲 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 水和过氧化氢的组成元素相同,则两者的化学性质相同 | |
| B. | 铝的金属活动性比铁强,则铝制品比铁制品更容易锈蚀 | |
| C. | 中和反应生成盐和水,生成盐和水的一定是中和反应 | |
| D. | 分子在不断地运动,原子也在不断地运动 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 为比较相同浓度的FeCl3溶液和CuSO4溶液对H2O2分解的催化效果,某研究小组进行了如下探究:
为比较相同浓度的FeCl3溶液和CuSO4溶液对H2O2分解的催化效果,某研究小组进行了如下探究:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com