
分析 粗盐提纯是通过溶解(把不溶物与食盐初步分离)、过滤(把不溶物彻底除去)、蒸发(食盐从溶液中分离出来而得到食盐的过程),据此确定三次用到的玻璃仪器.依次加入过量的NaOH溶液、过量的Na2CO3溶液,过滤后,滤液是氯化钠、氢氧化钠、碳酸钠的混合溶液,据此进行分析解答即可.
解答 解:粗盐提纯是通过溶解把不溶物与食盐初步分离,过滤把不溶物彻底除去,蒸发把食盐从溶液中分离出来而得到食盐的过程,其操作顺序应为溶解-过滤-蒸发.在溶解、过滤、蒸发操作中都要用到的玻璃仪器是玻璃棒.
提纯后的食盐中还含有少量的CaCl2和MgCl2等可溶性杂质.可将该食盐溶解后,依次加入过量的NaOH溶液、过量的Na2CO3溶液,过滤后,滤液是氯化钠、氢氧化钠、碳酸钠的混合溶液,向滤液中加入盐酸调节至pH=7,恰好完全反应,再将滤液蒸发结晶,即可得到更纯的氯化钠;NaOH溶液与盐酸反应氯化钠和水,反应的化学方程式为:HCl+NaOH=NaCl+H2O.
故答案为:玻璃棒;7;HCl+NaOH=NaCl+H2O.
点评 本题难度不大,熟练掌握粗盐的提纯的一般步骤、所需仪器、盐的化学性质等是正确解答本题的关键.


科目:初中化学 来源: 题型:解答题
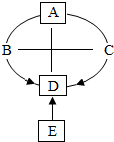 如图是初中化学常见的五种物质间的转化及反应关系(部分反应物或生成物及反应条件已略去)
如图是初中化学常见的五种物质间的转化及反应关系(部分反应物或生成物及反应条件已略去)查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 氯化钠是生活中重要的调味品,也是一种重要的工业原料.
氯化钠是生活中重要的调味品,也是一种重要的工业原料.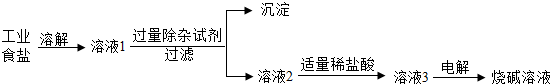
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
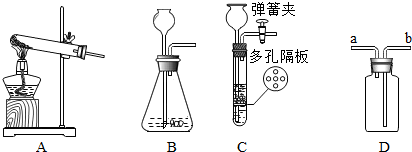
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
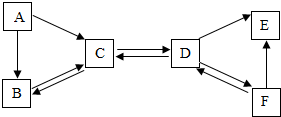 A、B、C、D、E、F是初中化学常见物质.A为单质,常溫下B、C均为气体,且B是一种大气污染物.D、F的溶液均能使无色酚酞溶液变红,E是厨房常用的一种调味品.它们之间的转化关系如图所示.请回答下列问题.
A、B、C、D、E、F是初中化学常见物质.A为单质,常溫下B、C均为气体,且B是一种大气污染物.D、F的溶液均能使无色酚酞溶液变红,E是厨房常用的一种调味品.它们之间的转化关系如图所示.请回答下列问题. 查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com