
| A. | 用闻气味的方法区别氧气和二氧化碳 | |
| B. | 用肥皂水鉴别硬水和软水 | |
| C. | 用稀硫酸区分黄铜(Cu、Zn)和黄金 | |
| D. | 用石灰水鉴别氢气和二氧化碳 |
分析 鉴别不同物质时,要根据物质的不同性质进行区分,现象要明显,方法要简便;主要通过颜色变化、是否有气泡冒出,是否有沉淀产生等现象来区别.
A、氧气和二氧化碳都是无味的气体;
B、肥皂水加入硬水中产生的泡沫较少;
C、锌能和稀硫酸反应,金和稀硫酸不反应;
D、石灰水能够和二氧化碳反应产生沉淀.
解答 解:A、用闻气味的方法不能区别氧气和二氧化碳,因为它们都是无色无味的气体,不能鉴别,故符合题意;
B、硬水和软水--加肥皂水,产生泡沫多的是软水,泡沫少或没有的是硬水,可以鉴别,故不合题意;
C、黄铜中含有锌,能和稀硫酸反应,金和稀硫酸不反应,可以鉴别,故不合题意;
D、氢气不能使澄清的石灰水变浑浊,而二氧化碳能使澄清的石灰水变浑浊,可以鉴别,故不符合题意;
故选A.
点评 本题主要考查不同物质的性质和鉴别,根据物质的性质差异以及物质间反应的实验现象进行分析解答即可.


 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
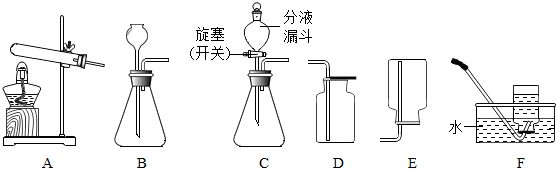
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
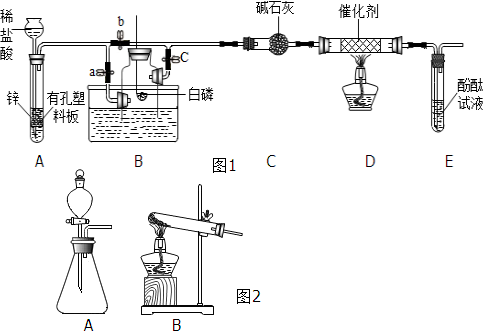
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 一个分子中含有9个水分子 | |
| B. | 氢元素和氧元素的质量比为2:1 | |
| C. | 氢元素的质量分数最大 | |
| D. | 在一定条件下,可燃烧生成CO2和H2O |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
 具有百年历史的滨州线松花江铁路大桥经维修后重新开放,桥面铺设了钢化玻璃,透过玻璃可直接俯瞰下面的铁轨、枕木、钢梁等原桥风貌及江面,成为了中东铁路公园一道亮丽的风景线,下列有关叙述正确的是( )
具有百年历史的滨州线松花江铁路大桥经维修后重新开放,桥面铺设了钢化玻璃,透过玻璃可直接俯瞰下面的铁轨、枕木、钢梁等原桥风貌及江面,成为了中东铁路公园一道亮丽的风景线,下列有关叙述正确的是( )| A. | 钢化玻璃属于金属材料 | |
| B. | 钢轨所用材料是锰钢,主要成分为铁、铬、镍,利用了其韧性好、硬度大的性能 | |
| C. | 为防止钢梁生锈可在钢梁表面刷漆 | |
| D. | 枕木的主要成分中含有纤维素,纤维素属于蛋白质 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 如图是A、B、C三种固体物质的溶解度曲线,根据该图回答下列问题.
如图是A、B、C三种固体物质的溶解度曲线,根据该图回答下列问题.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com