
| A. | 木炭在氧气中燃烧,发出白光,放出热量,产生能使澄清石灰水变白色浑浊的气体 | |
| B. | 硫在氧气中燃烧发出蓝紫色火焰,生成二氧化硫气体 | |
| C. | 红磷在空气中燃烧,产生黄白色火焰,放热,产生大量的白色烟雾 | |
| D. | 铁丝在空气中剧烈燃烧,火星四射,放热,生成黑色固体 |
分析 A、根据木炭在氧气中燃烧的现象进行分析判断.
B、根据硫在氧气中燃烧的现象进行分析判断.
C、根据红磷燃烧的现象进行分析判断.
D、根据铁丝在空气中不能燃烧进行分析判断.
解答 解:A、木炭在氧气中燃烧,发出白光,放出热量,产生能使澄清石灰水变白色浑浊的气体,故选项说法正确.
B、硫在氧气中燃烧生成二氧化硫气体属于结论,不是现象,故选项说法错误.
C、红磷在空气中燃烧,产生黄白色火焰,放热,产生大量的白烟,但没有雾,故选项说法错误.
D、铁丝在空气中不能燃烧,故选项说法错误.
故选:A.
点评 本题难度不大,掌握常见物质燃烧的现象即可正确解答;在描述物质燃烧的现象时,需要注意光和火焰、烟和雾、实验结论和实验现象的区别.


 考前必练系列答案
考前必练系列答案科目:初中化学 来源: 题型:填空题
| 物质 | 食醋 | 牛奶 | 食盐水 | 牙膏 | 肥皂水 |
| pH | 2~3 | 6~7 | 7 | 8~9 | 9~10 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
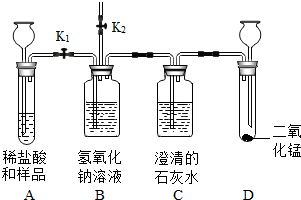 现有一份由碳酸钠和氯化钠组成的固体样品.初三化学兴趣小组的同学设计了图中的装置,请你与他们一起探究.
现有一份由碳酸钠和氯化钠组成的固体样品.初三化学兴趣小组的同学设计了图中的装置,请你与他们一起探究.查看答案和解析>>
科目:初中化学 来源: 题型:填空题
 图为铁丝在氧气和空气中燃烧的现象,根据要求回答下列问题:
图为铁丝在氧气和空气中燃烧的现象,根据要求回答下列问题:查看答案和解析>>
科目:初中化学 来源: 题型:解答题
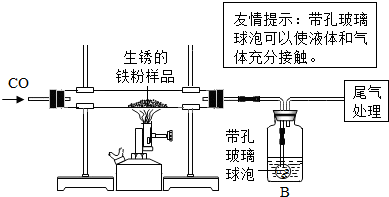 学了炼铁原理后,小明想用此原理测定某一生锈铁粉中氧化铁的质量分数.于是他取m1g生锈的铁粉样品,按下图所示装置进行实验,测定该样品中氧化铁的质量分数(铁锈按氧化铁处理).
学了炼铁原理后,小明想用此原理测定某一生锈铁粉中氧化铁的质量分数.于是他取m1g生锈的铁粉样品,按下图所示装置进行实验,测定该样品中氧化铁的质量分数(铁锈按氧化铁处理).查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 将燃着的木条伸入集气瓶中,检验CO2是否收集满 | |
| B. | 用向下排气法收集一瓶CO2气体,观察CO2的颜色 | |
| C. | 将CO2气体通入紫色石蕊试液中,证明CO2的水溶液显酸性 | |
| D. | 将CO2气体通入CaCl2溶液中,可以看到有白色沉淀生 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 实验序号 | 实验1 | 实验2 | 实验3 |
方案 | 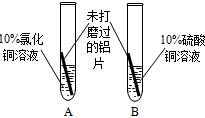 | 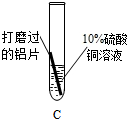 | 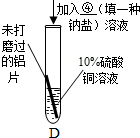 |
| 现象 | A中铝片表面有红色固体析出;B中铝片无明显现象 | ②铝片表面有红色固体析出 | 与A中的现象相同 |
| 结论 | 溶液中对氧化膜产生了破坏作用的离子可能是 ①Cl-(氯离子) | 除去表面氧化膜的铝片会与CuSO4溶液反应.该反应的化学方程式:③ 2A1+3CuSO4═A12(SO4)3+3Cu | 验证了实验1的结论 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com