
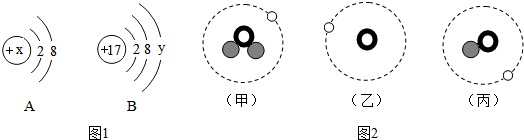
 道耳顿模型特点:不可再分的实心球体
道耳顿模型特点:不可再分的实心球体  汤姆生模型特点:正负电荷均匀分布
汤姆生模型特点:正负电荷均匀分布 卢瑟福模型特点:核位于原子中心,质量集中在核上.
卢瑟福模型特点:核位于原子中心,质量集中在核上. ”表示质子,“
”表示质子,“ ”表示中子,“○”表示电子.请通过比较归纳:
”表示中子,“○”表示电子.请通过比较归纳:分析 (1)根据已有的知识进行分析解答,根据当核电荷数=质子数=核外电子数,为原子进行解答;
(2)根据在原子中,核内质子数=核外电子数进行解答;
(3)最外层电子数小于4的在化学反应中易失去电子形成阳离子;据此解答;
(4)根据化合物名称的读法写出其名称即可;
(5)根据已有的原子的构成以及α粒子散射实验的现象进行分析解答即可;
(6)质子数相同的同一类原子为同种元素;质子数为1的元素为氢元素;
(2)对比三种粒子构成上的异同点,归纳粒子构成的规律等.
解答 解:(1)根据当核电荷数=质子数=核外电子数,为原子,故A表示氖原子元素符号为Ne,故填:Ne;
(2)当核电荷数=质子数=核外电子数,为原子,所以若B表示某原子的结构示意图,则y=17-2-8=7;故填:7;该元素的原子在化学反应中容易得到电子.
(3)A是阳离子的结构示意图,则x>10,故填:CD.
(4)A中x=13,则A是铝元素,该结构示意图是铝离子,B是氯元素,形成的是氯离子,故形成的化合物是氯化铝,故填:氯化铝,AlCl3;
(5)①若原子质量、正电荷在原子内均匀分布,则极少数α粒子就不会发生大角度散射.原子中“很小的结构”指的是原子核;
②绝大多数α粒子穿过后方向不变,说明原子内部绝大部分空间是空的,故填:B;
通过α粒子散射实验,得出的是原子有核模型,故填;C.
(6)粒子甲的核内有一个质子和两个中子,粒子乙的核内只有一个质子而无中子,丙的核内有一个质子和一个中子,因此甲、乙、丙在原子结构上的区别是原子中所含中子数不同;
三种粒子都只有一个质子,可判断同属于氢元素;
答案:
(1)Ne;
(2)7;得到;
(3)cd;
(4)AlCl3;
(5)①原子核;②B;C.
(6)原子中所含中子数不同;氢.
点评 本题考查的是原子结构的知识,完成此题,可以依据已有的知识进行.掌握原子结构示意图以及有关的意义是解答本题的关键.


 寒假天地重庆出版社系列答案
寒假天地重庆出版社系列答案科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:选择题

| A. | 反应前后各物质均由分子构成 | B. | 该反应为分解反应 | ||
| C. | 反应前后原子的数目不变 | D. | 反应前后均为混合物 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 构成物质的粒子有分子、原子和离子 | |
| B. | 空气中含量最多的气体是氮气 | |
| C. | 一种元素在同一化合物只显示一种化合价 | |
| D. | 水通电后生成氢气和氧气,说明在化学变化中分子可以再分 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 明矾溶液可以区分硬水和软水 | |
| B. | 自来水厂净化水的过程,发生的变化都是物理变化 | |
| C. | 为了节约用水,可以用工业废水直接浇灌农田 | |
| D. | 水与过氧化氢的组成元素相同,均可通过化学反应生成氧气 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
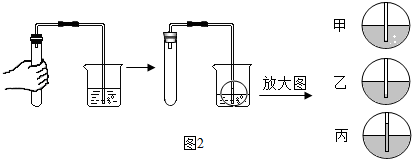
 实验室用块状大理石和6mol/L的盐酸为试剂,利用如图部分仪器或物品,设计两套随开随制,随关随停的CO2的简易发生装置(不考虑夹持或支撑仪器),在横线上填写有关仪器(或物品)的编号:②⑤⑥⑦或者是③⑥⑦.
实验室用块状大理石和6mol/L的盐酸为试剂,利用如图部分仪器或物品,设计两套随开随制,随关随停的CO2的简易发生装置(不考虑夹持或支撑仪器),在横线上填写有关仪器(或物品)的编号:②⑤⑥⑦或者是③⑥⑦.查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| 选项 | 待提纯的物质 | 操作方法 |
| A | O2(H2O) | 将混合气体通过盛有足量浓硫酸的洗气瓶 |
| B | Cu(CuO) | 加入足量的稀硫酸、过滤、洗涤、干燥 |
| C | CaCO3(NaCl) | 加足量水溶解、过滤、蒸发、结晶 |
| D | ZnSO4溶液(FeSO4) | 加入足量的锌粉,过滤 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com