
将8.1g氧化锌固体放入100g稀硫酸中,恰好完全反应。试计算:
①可生成硫酸锌多少克?
②所用稀硫酸的溶质质量分数是多少?
(温馨提示:化学方程式:ZnO + H2SO4 = ZnSO4 + H2O)
 鸿图图书寒假作业假期作业吉林大学出版社系列答案
鸿图图书寒假作业假期作业吉林大学出版社系列答案科目:初中化学 来源: 题型:
最近新疆乌鲁木齐某在建小区附近出现了“火 山”,是地下浅表煤层在岩石裂缝处发生的自燃现象。要熄灭该煤层的燃烧,你提出的办法是____。该煤层自燃的过程中会产生大量的可燃性气体,该气体的化学式为____;实验室点
山”,是地下浅表煤层在岩石裂缝处发生的自燃现象。要熄灭该煤层的燃烧,你提出的办法是____。该煤层自燃的过程中会产生大量的可燃性气体,该气体的化学式为____;实验室点 燃该气体前必须要对气体进行____。
燃该气体前必须要对气体进行____。
查看答案和解析>>
科目:初中化学 来源: 题型:
丁二酮(C4H6O2)可用作糖果增香剂.下列关于丁二酮的说法中正确的是( )
|
| A. | 丁二酮属于有机高分子化合物 |
|
| B. | 丁二酮中含有氧原子 |
|
| C. | 丁二酮中氧元素的质量分数最大 |
|
| D. | 丁二酮中氢元素的质量分数为6.98% |
查看答案和解析>>
科目:初中化学 来源: 题型:
有甲、乙、丙、丁四种金属。只有甲在自然界主要以单质形式存在。丁盐的水溶液不能用乙制的容器盛放,但可用丙制的容器盛放。这四种金属的活动性由强到弱的顺序是
A.甲>乙>丁>丙 B. 乙>丁>丙>甲 C.丙>乙>丁>甲 D.  丙>丁>乙>甲
丙>丁>乙>甲
查看答案和解析>>
科目:初中化学 来源: 题型:
某同学用空塑料饮料瓶做简易净水器,设计如图。


(1)小卵石、石英沙和膨松棉的作用是 ; 活性炭的作用是 。
(2)净化后是硬水还是软水,可用___________________来检验。
(3)长期饮用硬水对人体健康不利,要降低水的硬度,可采用 _方法。
查看答案和解析>>
科目:初中化学 来源: 题型:
为除去物质中的少量杂质,选用的试剂及操作均正确的一组是
| 选项 | 物质 | 杂质 | 选用的试剂 | 选用的操作 |
| A | CO2 | H2O蒸气 | 固体NaOH | 通过盛NaOH的U型管 |
| B | CuSO4粉末 | Fe粉 | 水 | 加水,搅拌、过滤、蒸发 |
| C | O2 | H2O蒸气 | 足量浓硫酸 | 洗气 |
| D | NaHCO3粉末 | Na2CO3粉末 | 适量稀盐酸 | 滴加后蒸发 |
查看答案和解析>>
科目:初中化学 来源: 题型:
有一包“铁”的粉末,可能含有Fe 、Fe2O3 Fe3O4 中的一种或几种,现称取23.2g放在试管中,通入足量的一氧化碳并加热充分反应,将生成的气体全部通入足量的澄清石灰水,共得到40g的碳酸钙固体。关于这包“铁” 的粉末成分判断正确的是
A.一定是纯净物 B.一定有Fe 、Fe2O3 Fe3O4三种
C.如果有Fe ,就一定有Fe2O3 D.如果有Fe2O3 ,就一定有Fe3O4
查看答案和解析>>
科目:初中化学 来源: 题型:
兴趣小组欲测定某未知浓度Ba(OH)2溶液的溶质质量分数,请你和他们一起完成实验并回答有关问题.
(1)配制30g 10%的Na2CO3溶液 .
.
步骤为:计算、称取、量取、 、转移.量取水时应选用规格为 mL(从10、50、100中选取)的量筒.最后将碳酸钠溶液转移到试剂瓶中,贴上标签备用,在标签上可以不必注明的是 (填序号).
A.30g B.10% C.Na2CO3溶液
(2)测定未知浓度Ba(OH)2,溶液的溶质质量分数.
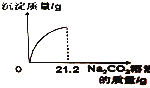
取50g Ba(OH)2溶液,逐滴滴加上述Na2CO3溶液的过程中,测得产生沉淀与加入Na2CO3溶液的质量关系如图所示.
①恰好完全反应时,消耗Na2CO3溶液的质量为 g.
②请通过计算确定Ba(OH)2溶液的溶质质量分数.
查看答案和解析>>
科目:初中化学 来源: 题型:
氯化铁是常见的水处理剂。以硫铁矿(主要成分为FeS2)为原料制备氯化铁晶体(FeCl3•6H2O)的工艺流程如下:

回答下列问题:
(1)硫铁矿在空气中焙烧流程中生成氧化铁和二氧化硫,请将硫铁矿和空气反应的化学方程式补充完整:4FeS2 + 11X= 2Fe2O3 + 8SO2,则物质X的化学式为________________。
(2)大量排放出的二氧化硫能形成 ,危害环境。可将含二氧化硫的废气通入呈碱性的氨水中吸收二氧化硫,则氨水的pH_______7(填写“大于”、“小于”或“等于”)。
(3)在实验室中,欲用38%(密度为1.18g/mL)的盐酸配制30%的盐酸,则需要的玻璃仪器有__________、_________(填两种仪器名称)。
(4)上述流程中需用30%的盐酸“酸溶”焙烧后的残渣(主要成分是氧化铁),写出该反应的化学方程式__ _____________________________________,属于_________
_____________________________________,属于_________ _反应。
_反应。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com