
| 序号 | 实验操作 | 主要实验现象 | 实验结论和解释 |
| ① | 取少量该溶液于一支试管中,向其中滴加2-3滴无色酚酞试液. | 无色酚酞试液变红 | 该溶液不可能是______.理由是______. |
| ② | 另取少量该溶液于一支试管中,向其中滴加足量的稀盐酸. | ______. | 溶液中一定含有的溶质是碳酸钠,有关反应的化学方程式为______. |
| 实验操作 | 主要实验现象 | 实验结论和解释 |
| ______. | ______. | 该溶液是氢氧化钠溶液. |
| 序号 | 实验操作 | 主要实验现象 | 实验结论和解释 |
| ① | 该溶液不可能是NaCl.理由是只有NaCl溶液不能使酚酞变红. | ||
| ② | 有气泡产生. | 有关反应的化学方程式为:Na2CO3+2HCl=2NaCl+CO2↑+H2O. |
| 实验操作 | 主要实验现象 | 实验结论和解释 |
| 取少量该溶液于一支试管中,向其中加入足量的CaCl2溶液,再滴加酚酞. | 产生白色沉淀,滴酚酞后变红. |


 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源: 题型:阅读理解
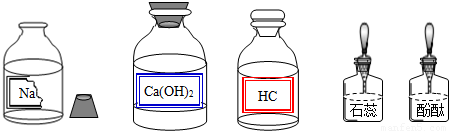
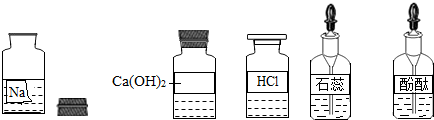
 某校兴趣小组同学准备进行常见的酸、碱、盐的性质实验时,发现实验台上摆放的药品中有一个装溶液的试剂瓶未盖瓶盖且标签破损(如图),于是决定对这瓶溶液进行实验探究:
某校兴趣小组同学准备进行常见的酸、碱、盐的性质实验时,发现实验台上摆放的药品中有一个装溶液的试剂瓶未盖瓶盖且标签破损(如图),于是决定对这瓶溶液进行实验探究:查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解


查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解

查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解


查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com