
【题目】下图是在一定条件下,某物质发生化学反应的微观模拟图,请从微观角度回答下列问题:
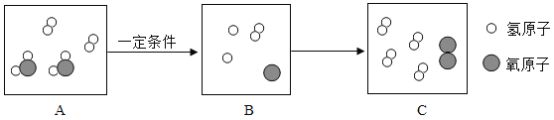
(1)请在B图中补充相关粒子图形,使其表示正确____;
(2)此反应前后,反应物分子与各生成物分子的最简个数比为____________;
(3)C图是由两种单质组成的混合物的微观理由是_________________;
(4)画出比氧元素多一个周期且能与氧元素形成“AB”型化合物的元素离子结构示意图___________。
【答案】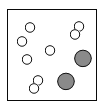 2:2:1 由两种分子构成,且每一种分子都只含有一种的原子
2:2:1 由两种分子构成,且每一种分子都只含有一种的原子 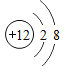
【解析】
由物质发生化学反应的微观模拟图中可知,反应是水一定条件下生成氢气和氧气。
(1)由质量守恒定律化学反应前后原子的种类和个数不变可知,在B图中应补充两个氢原子、一个氧原子和一个氢分子,故粒子图形为 。
。
(2)反应的化学方程式为 ,故此反应前后,反应物分子与各生成物分子的最简个数比为2:2:1。
,故此反应前后,反应物分子与各生成物分子的最简个数比为2:2:1。
(3)C图是氢气和氧气,氢气分子是由氢原子构成的,氧气分子是由氧原子构成的,故由两种单质组成的混合物的微观理由是由两种分子构成,且每一种分子都只含有一种的原子。
(4)比氧元素多一个周期且能与氧元素形成“AB”型化合物的元素是镁元素,易失去最外层2个电子形成镁离子,故镁离子结构示意图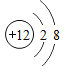 。
。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:初中化学 来源: 题型:
【题目】在高温条件下,A、B 两种物质可以发生化学反应生成C 和D。反应前后分子种类变化的微观示意图如图所示。在这个化学反应中,以下叙述正确的是 ( )
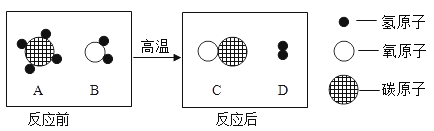
A.该反应是化合反应B.物质 B 的相对分子质量是 16
C.生成C 和D 的微粒个数比 1:1D.生成C 和D 的质量比是 14:3
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】我国科学家侯德榜,在氨碱法的基础上,创立了更为先进的联合制碱法生产纯碱碳 酸钠。某海边工厂利用贝壳、海盐等生产纯碱的主要工艺流程如下:
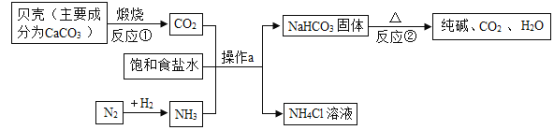
(1)反应①的化学方程式为_____。反应②属于_____反应(填基本反应类型)。
(2)工业上常用_____的方法制取氮气,该过程属于_____变化。
(3)操作 a 的名称是_____,实验室在进行该操作时,用到的玻璃仪器有烧杯、漏斗和_____。
(4)在工农业生产过程中,会排放 CO2 加剧温室效应。下列做法能减少二氧化碳排放的是_____(填序号)。
a 焚烧秸秆肥田 b 提高火力发电量 c 大力使用清洁能源
(5)有一种处理 CO2 的方法,是将 CO2 与氢气在一定条件下反应生成甲烷和水,该反应的化学方程式 为:_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】学习小组测定某工业废水中 H2SO4的含量。取 100g 废水于烧杯中,加入200gBaCl2 溶液,恰好完全反应,经过滤得到 253.4g 溶液(H2SO4 + BaCl2 = BaSO4 ↓+2HCl)(可溶性杂质不参加反应,过滤后滤液的损失忽略不计)
(1)充分反应后生成沉淀的质量为______g;
(2)该工业废水中硫酸的质量分数为____________?(写出计算过程)
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】化学兴趣小组用一瓶久置的过氧化氢溶液制取氧气并测量过氧化氢质量分数。称量68g过氧化氢溶液和0.1g二氧化锰进行实验,反应前后质量液体和二氧化锰质量随时间变化关系如下图。计算:
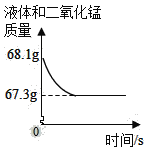
(1)制得氧气的质量是_____g。
(2)该过氧化氢溶液中溶质的质量分数是多少?____(写出计算过程)
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】实验室有一瓶失去标签的溶液,知道只含有一种阳离子钾离子,为了弄清其到底含有几种溶质(都是初中常见的物质),四九芳华小组做了如下实验:(不考虑微溶和碳酸氢根)
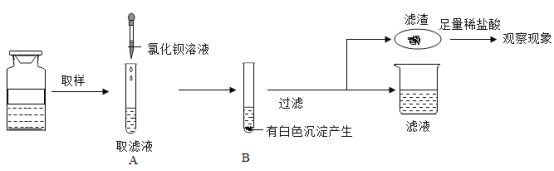
根据上述实验过程:小四同学根据滤渣处产生的_____________现象,从而确定了一定含有的两种溶质为___________,写出此过程反应的化学方程式:________。
还有那些溶质呢?小九同学继续探究如下图:
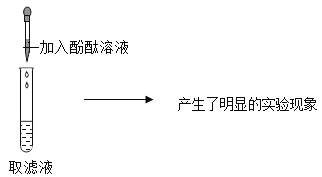
得出结论:该溶液一定含有氢氧化钾,请你对其结论进行评价_________;四九芳华小组经过讨论,觉得上述过程所加的试剂有一处不够明确和准确,从而对后续其他溶质的确定带来了影响,决定对一种试剂稍作调整,其他不变,调整为__________________,然后重新取滤液加入________,立即向所得溶液中加入__________,从而可推出瓶中溶液的溶质最多有__________种。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】根据下图分别回到问题
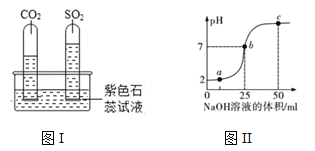
(1)如图 I,已知: SO2 气体是空气的污染物之一,和 CO2 性质相似。如图所示,水槽中盛有紫色石蕊试液,将收集满两种气体的试管同时倒立于其中,片刻后实验现象如图所示,试管内液体都变成红色。从实验现象中可以得出 SO2 气体一条物理性质____。写出SO2 与水反应的化学方程式___。SO2 气体也能使澄清石灰水变浑浊,写出该反应的化学方程式____。
(2)如图 II,向盛有稀盐酸的烧杯中逐滴加入 NaOH 溶液,测得烧杯中溶液的 pH 变化如图所示。写出反应的化学方程式____。C 点处溶液中存在的离子有___。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】李婉仪同学在做 NaOH 溶液与 CuSO4 溶液反应的实验时,观察到有蓝色沉淀生成,对该沉淀进行加热,一般会看到蓝色沉淀变成黑色,可有时却看到蓝色沉淀变成绿色。李同学对此异常现象产生了兴趣,决定对此现象产生的实验条件进行探究。
(查阅资料)难溶性碱受热易分解成对应的金属氧化物。写出上述生成蓝色沉淀以及蓝色沉淀变成黑色的化学反应方程 ________________、______________。
(提出问题)加热蓝色沉淀产生黑色固体与什么因素有关?
(作出猜想)猜想 1:与 CuSO4 溶液过量有关;猜想 2:与 NaOH 溶液过量有关。
(设计实验)限选试剂:1%NaOH 溶液,20%NaOH 溶液,1%CuSO4 溶液,20%CuSO4 溶液。
实验方案 | 实验现象 | 实验结论 |
(1)向 2 mL 20%CuSO4 溶液中滴加 2 滴 1%NaOH 溶液,再将所得沉淀加热 | 先产生蓝色沉淀,加热后___________。 | 猜想 1 成立 |
(2)_______________,再将所得沉淀加热 | 先产生蓝色沉淀,加热后___________。 | 猜想 2 不成立 |
(得到结论)在上述实验中,要能观察到蓝色沉淀变成黑色,关键是________。
(拓展与思考)进一步查阅资料得知,上述绿色物质是溶解度比氢氧化铜更小的水胆矾[化学式为Cu4(OH)6SO4],该物质能与酸反应,形成蓝色溶液。李同学想设计一个实验,证明该绿色物质中含有硫酸根,于是将上述绿色物质用蒸馏水洗涤、烘干,再溶解在足量的溶液 A 中,向所得溶液中滴加溶液 B,若有白色沉淀生成,则表示原绿色物质中有硫酸根。试推测:溶液 A 中溶质的化学式是______,溶液 B 中溶质的化学式是___________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某化学兴趣小组为探究化学反应中的能量变化,进行以下实验:
(探究一)盐酸与氢氧化钠的反应
(1)写出氢氧化钠溶液与盐酸反应的化学方程式:_________________________________。
(2)甲同学设计实验:向一定量氢氧化钠固体中倒入20mL 4%盐酸,用温度计测量反应前后各溶液的温度。乙同学认为该实验方案不合理,其理由是_________________________。
(3)丙同学设计了如下三组实验,请你帮助他完成实验方案:
实验编号 | 实验方案 |
实验1 | 向20mL 4%盐酸中倒入20mL水,测定稀释前后溶液的温度。 |
实验2 | 向20mL 5%氢氧化钠溶液中________________,测定稀释前后溶液的温度。 |
实验3 | _______________________________________________________________。 |
(4)丙同学观察到的实验现象是:实验3溶液升高的温度远大于实验1与实验2溶液升高的温度之和,由此你能得出的实验结论是①____________;②____________。
(探究二)盐酸与碳酸氢钠溶液的反应。
下图是丁同学在20℃、基本隔热条件下利用温度传感器,分别测定向20mL水和20mL饱和碳酸氢钠溶液中各倒入20mL 13.7%盐酸的温度与时间变化曲线。
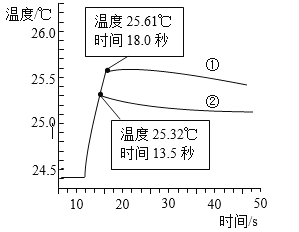
曲线①为水+13.7%盐酸温度变化曲线
曲线②为饱和碳酸氢钠溶液+13.7%盐酸温度变化曲线
实验测得饱和碳酸氢钠溶液稀释时温度变化不大,可忽略不计,据此回答下列问题:
(5)18.0秒后,曲线①逐渐下降的原因是____________________________________;
(6)比较曲线①和曲线②,你认为13.7%盐酸与饱和碳酸氢钠溶液的反应是________(填“放热”或“吸热”)反应,其理由是_________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com