
某碳酸钙和氧化钙组成的混合物中钙元素的质量分数为 60%,将50g 该混合物高温煅烧至固体质量不再改变,则生成二氧化碳的质量是
A.6g B.8g C.13.2g D.20g
 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源: 题型:
将40g碳酸钙高温煅烧一段时间后,冷却测得剩余固体质量为35.6g,再向剩余固体中加入足量稀盐酸,充分反应后,蒸发结晶,理论上可得到固体氯化钙的质量为( )
|
| A. | 无法确定 | B. | 44.4g | C. | 33.3g | D. | 35.6g |
查看答案和解析>>
科目:初中化学 来源: 题型:
根据下图有关信息判断,下列说法错误的是()
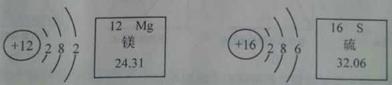
A.在元素周期表中,镁元素和硫元素属于同一周期
B.镁离子核内有12个质子
C.在化学反应中,硫原子容易失去2个电子
D.硫元素的原子序数为16
查看答案和解析>>
科目:初中化学 来源: 题型:
化学是一门富有创造性的科学.含氟物质的合成,对推动社会进步发挥着巨大作用.
(1)如图是氟元素在元素周期表中的相关信息,画出氟元素的原子结构示意图 ,由氟原子的结构示意图知,氟原子在化学反应中易 得 (填“失”或“得”)电子.
(2)氟化钠常用作牙膏添加剂,能有效预防啮齿.氟化钠和氯化钠一样,都是由 (填“分子”、“原子”或“离子”)构成.
(3)被誉为“塑料王”的聚四氟乙烯,常用不粘锅锅底涂层,它的化学性质非常稳定,不与油、盐、醋等反应.从材料分类角度看,塑料是一类 材料,从人体所需营养素角度看,油、盐、醋中的“油”指的是 .
(4)氟利昂曾经是一种横好的制冷剂,自1987年国际规定禁止使用,因为氟利昂分解出氟原子能引发下列循环反应而破坏臭氧(O3)层:①Cl+O3=ClO2②ClO+O3=Cl+O2.在上述循环反应中氯原子起 作用,O3和O2的化学性质不同的原因是 .

查看答案和解析>>
科目:初中化学 来源: 题型:
2016年5月4日,北京的王女士因混合使用洁厕灵(盐酸)和84消毒液(次氯酸钠)清洁马桶,中毒死亡。其原因是2HCl+NaClO=NaCl+Cl2↑+H2O 产生的氯气有毒。
⑴上述反应中,氯元素化合价最高的物质是(填字母)。
A.HCl B.NaClO C.NaCl D.Cl2
⑵符号“Cl2”的意义是 (答出一条即可)。
⑶《生活饮用水卫生标准》中,允许自来水厂使用氯气对天然水进行灭菌消毒,在此之前还要经过沉降、 等净化操作;要求水的总硬度(以碳酸钙计)不超过450mg/L,生活中降低水的硬度的常用方法是 煮沸 。
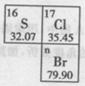

⑷已知溴元素(Br)的原子结构示意图为 ,那么,溴原子核内
质子数为,溴原子易 电子(填“得到”或“失去”)。
⑸氯和溴两种元素在周期表中的位置见右图,二者属于同一 (填“周期”或“族”)。
查看答案和解析>>
科目:初中化学 来源: 题型:
二氧化硫是一种无色具有刺激性气味的气体,它进入大气后可形成硫酸型酸雨。
⑴煤、石油、木柴中都含有硫元素,点燃后均会产生二氧化硫气体,可用 ▲ 溶液检
验该气体的存在。
⑵为减少大气污染,火力发电厂采用以下两种方法吸收废气中的二氧化硫。
①用氨水吸收废气中的二氧化硫,其反应原理可用化学方程式表示为 ▲ 。已知:亚硫酸盐不稳定,易被空气中的氧气氧化成硫酸盐。
②用石灰石浆吸收废气中的二氧化硫,其反应原理是:2CaCO3+O2+2SO2 2CaSO4+2CO2 。若1000kg废气中含有1.6kg的二氧化硫,则至少需要含90%碳酸钙的石灰石多少千克才能将其完全吸收(写出解题过程,计算结果保留一位小数)?
2CaSO4+2CO2 。若1000kg废气中含有1.6kg的二氧化硫,则至少需要含90%碳酸钙的石灰石多少千克才能将其完全吸收(写出解题过程,计算结果保留一位小数)?
查看答案和解析>>
科目:初中化学 来源: 题型:
为测定某氮肥中硫酸铵的纯度(及质量分数)是否与下图标签相符合,小林取15g该氮肥样品配成溶液,加入足量氯化钡溶液充分反应后,过滤、洗涤、烘干,测得沉淀质量为23.3g。试通过计算确定该氮肥中硫酸铵的纯度是否与标签相符。
 |
查看答案和解析>>
科目:初中化学 来源: 题型:
|
(1)发生反应的化学方程式为 Cu+2AgNO3=Cu(NO3)2+2Ag .
(2)试计算该合金中铜与银的质量比.(请写出计算过程)
(3)华雪同学认为还可算出该AgNO3溶液中溶质的质量分数,于是进行了多次实验,记录了每次使用AgNO3溶液的质量a(AgNO3溶液)和充分反应后所得固体的质量b,并绘制了如图,则AgNO3溶液中溶质的质量分数是多少?(请写出计算过程,用含m的代数式表示)【出处.

查看答案和解析>>
科目:初中化学 来源: 题型:
实验结束时,同学们将含有CuSO4、ZnSO4、FeSO4的废液倒在废液缸里,如果将废液直接排放就会造成水污染。于是几位同学利用课余处理废液,回收工业重要原料硫酸锌和有关金属。实验过程如下:
 |
请回答:
(1)滤液A和滤液B含有相同的溶质,其名称是 ;固体B的化学式为 。
(2)写出步骤①其中一个反应的化学方程式 ;步骤④发生反应的化学方程式为 。
(3)要检验步骤④中加入的稀硫酸是否足量的方法是
。
(4)若实验过程中的物质损失可以忽略,要计算该废液中硫酸锌的质量分数,必须称量:废液的质量和 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com