(2010?宿迁)某兴趣小组为了测定草木灰中K2CO3的含量,取现有草木灰69g,逐滴加入溶质质量分数为7.3%的稀盐酸至恰好完全反应(假设草木灰除K2CO3外,其他物质均不溶于水,也不与稀盐酸反应),生成标准状况下(0℃,l atm)的CO21.12L.试通过计算回答下列问题:
(1)设标准状况下,44g CO2气体的体积为22.4L,则1.12L CO2气体的质量是______g.
(2)加入稀盐酸的质量是______g.
(3)求草木灰中K2CO3的质量分数(写出解题过程).
【答案】
分析:根据反应的化学方程式,由生成二氧化碳气体的质量可计算出参加反应的HCl质量及碳酸钾的质量;
利用稀盐酸的质量=
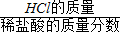
和草木灰中K
2CO
3的质量分数=

,完成后面的计算.
解答:解:(1)标准状况下,44g CO
2气体的体积为22.4L,则1.12L CO
2气体的质量=
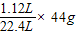
=2.2g
故答案为:2.2;
(2)设参加反应的HCl的质量为m
K
2CO
3+2HCl═2KCl+H
2O+CO
2↑
73 44
m 2.2g

m=3.65g
加入稀盐酸的质量=
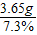
=50g
故答案为:50;
(3)设69g草木灰中含K
2CO
3的质量为x
K
2CO
3+2HCl═2KCl+H
2O+CO
2↑
138 44
x 2.2g

x=6.9g
该草木灰中含K
2CO
3的质量分数为
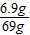
×100%=10%
答:该草木灰中含K
2CO
3的质量分数为10%.
点评:利用化学方程式表示反应中各物质的质量关系,由反应中某物质的质量完成反应中其它物质质量的计算,然后根据溶液的质量、混合物中化合物的含量等计算公式完成整个问题的计算.

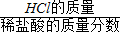 和草木灰中K2CO3的质量分数=
和草木灰中K2CO3的质量分数= ,完成后面的计算.
,完成后面的计算.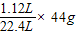 =2.2g
=2.2g
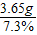 =50g
=50g
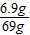 ×100%=10%
×100%=10%