
 测定空气中氧气含量的方法很多.如图是测定空气中氧气含量实验的装置图,我们九年级一班的化学兴趣小组同学们对该实验过程产生了意见的分歧,请你帮忙解决一下.
测定空气中氧气含量的方法很多.如图是测定空气中氧气含量实验的装置图,我们九年级一班的化学兴趣小组同学们对该实验过程产生了意见的分歧,请你帮忙解决一下.| 硬质玻璃管中空气的体积 | 反应前注射器中空气体积 | 反应后注射器中气体体积 | 实验测得空气中氧气的体积分数 |
| 25mL | 15mL | 7mL | 20% |
分析 (1)注射器内气体减少的量就是氧气的量;
(2)装置中气球的作用是:缓冲,防止试管内气体温度升高,气压增大,冲开橡皮塞.
解答 解:(1)注射器内气体减少的量就是氧气的体积,则实验测得空气中氧气的体积分数为:$\frac{15ml-7ml}{25ml+15ml}×100%$=20%;小亮的说法不对,反应前注射器中空气体积不能忽略;
(2)装置中气球的作用是:缓冲,防止试管内气体温度升高,气压增大,冲开橡皮塞.
故答案为:(1)20%;反应前注射器中空气体积不能忽略;
(2)缓冲,防止试管内气体温度升高,气压增大,冲开橡皮塞.
点评 合理设计实验,科学地进行实验、分析实验,是得出正确实验结论的前提,因此要学会设计实验、进行实验、分析实验,为学好化学知识奠定基础.


 寒假学与练系列答案
寒假学与练系列答案科目:初中化学 来源: 题型:选择题
| A. | K+、Na+、OH-、Cl- | B. | H+、Na+、NO3-、CO32- | ||
| C. | Ba2+、Cu2+、NO3-、SO42- | D. | H+、Ba2+、NO3-、OH- |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
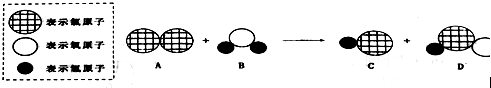
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
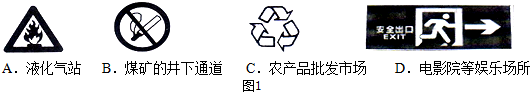
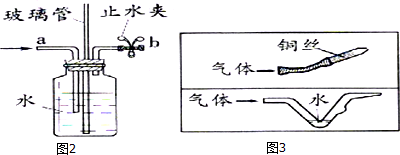
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 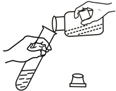 倾倒试剂 | B. |  滴加试剂 | C. | 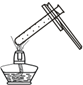 液体加热 | D. | 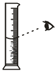 量筒读数 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
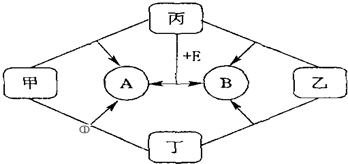
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com