
| 反应前 | 反应后 | |
| 烧杯和样品溶液总质量/g | 加入的氯化钡溶液质量/g | 过滤后烧杯和溶液总质量/g(滤液的损失忽略不计) |
| 95 | 65 | 140.3 |
分析 根据质量守恒定律可知,过程中质量的减少是因为生成了碳酸钡,所以可以求算碳酸钡的质量,根据碳酸钡的质量和对应的化学方程式求算碳酸钠的质量,进而求算氢氧化钠的质量分数.
解答 解:根据质量守恒定律可得,生成的碳酸钡的质量为95g+65g-140.3g=19.7g
设样品中碳酸钠的质量为x
BaCl2+Na2CO3=BaCO3↓+2NaCl
106 197
x 19.7g
$\frac{106}{197}$=$\frac{x}{19.7g}$
x=10.6g
样品中氢氧化钠的质量为15g-10.6g=4.4g
样品中氢氧化钠的质量分数为$\frac{4.4g}{15g}$×100%≈29.3%
由于反应前后钠元素都是以离子形式存在,没有减少,所以
在反应前后的溶液中,下列元素质量保持不变的是钠元素.
答:(1)A;
(2)反应共生成沉淀 19.7克;
(3)原样品中NaOH的质量分数约为29.3%.
点评 根据化学方程式计算时,第一要正确书写化学方程式,第二要使用正确的数据,第三计算过程要完整.


科目:初中化学 来源: 题型:推断题
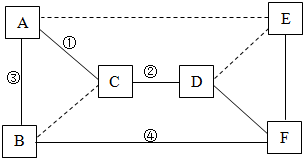 A~F是碳单质、氧化铜、二氧化碳、稀硫酸、氢氧化钠和碳酸钠六种物质中的某一种,A、B都是黑色固体,E属于盐,它们之间的相互关系如图所示(实连线“-”表示物质间能反应,虚连线“…”表示物质间不能反应).请回答下列问题:
A~F是碳单质、氧化铜、二氧化碳、稀硫酸、氢氧化钠和碳酸钠六种物质中的某一种,A、B都是黑色固体,E属于盐,它们之间的相互关系如图所示(实连线“-”表示物质间能反应,虚连线“…”表示物质间不能反应).请回答下列问题:查看答案和解析>>
科目:初中化学 来源: 题型:解答题
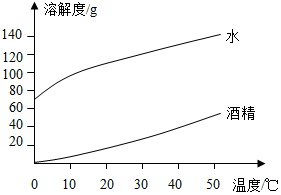 图表法是一种常用的数据处理方法,结合所给图表回答下列问题
图表法是一种常用的数据处理方法,结合所给图表回答下列问题| 氢氧化钠 | 碳酸钠 | |||
| 20℃ | 40℃ | 20℃ | 40℃ | |
| 水 | 109g | 129g | 21.8g | 49g |
| 酒精 | 17.3g | 40g | 不溶 | 不溶 |
查看答案和解析>>
科目:初中化学 来源: 题型:计算题

查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com