
| A. | Fe(OH)3,KOH | B. | Ba(NO3)2,CaCO3 | C. | MgSO4,K2CO3 | D. | CaO,Fe2O3 |
 名师金手指领衔课时系列答案
名师金手指领衔课时系列答案科目:初中化学 来源: 题型:选择题
| A. | 单质中只含有一种元素,因此只含有一种元素的物质一定是单质 | |
| B. | 碱性溶液能使酚酞试液变红色,因此能使酚酞试液变红色的溶液的pH一定大于7 | |
| C. | 中和反应生成盐和水,由此推断生成盐和水的反应一定是中和反应 | |
| D. | 稀有气体元素的原子最外层电子数为8(氦除外),因此微粒 一定是稀有气体元素的原子 一定是稀有气体元素的原子 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 盐酸、硫酸都能使石蕊溶液变红,是因为溶液中都含有氢离子 | |
| B. | 金属镁在空气中比铝更容易燃烧,是因为镁比铝的活动性强 | |
| C. | 用稀盐酸或灼烧的方法区分真黄金和假黄金(铜锌合金) | |
| D. | 滴加氯化钡溶液有白色沉淀生产,证明原溶液中一定含有CO${\;}_{3}^{2-}$或SO${\;}_{4}^{2-}$ |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
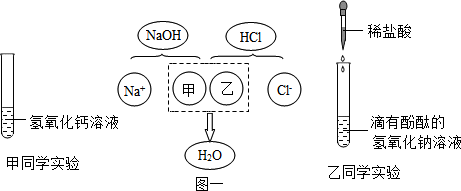
| 实验操作 | 实验现象 | 实验结论 |
| 取样少许于试管中,先滴加 过量CaCl2溶液[或BaCl2、Ba(NO3)2、Ca(NO3)2],再滴加 酚酞溶液 | 有白色沉淀生成, 酚酞溶液变红. | 氢氧化钠溶液部分变质 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 煤为人类提供能源和化工原料的同时,也埋下了祸根 | |
| B. | 氢气让人欢喜让人忧 | |
| C. | 煤气化能提高市民的生活质量,同时也是个潜伏着的无形杀手 | |
| D. | 水是取之不尽的,只有个别地区存在着用水危机 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题

查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com