
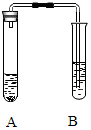
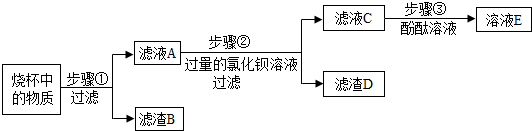
分析 【现象分析】氢氧化钠溶于水放出热量,氧化钙与水反应会放出热量;
【探究运用】根据碳酸钠能与氢氧化钡反应来分析;
(1)根据实验过程中的现象以及溶液的酸碱性来分析;
(2)根据碳酸钡能溶于酸,硫酸钡不溶于酸来分析.
解答 解:【现象分析】氢氧化钠溶于水放出热量,氧化钙与水反应会放出热量,会觉得左侧试管外壁发热,观察到右侧试管的导管口处有气泡冒出;氢氧化钠溶于水属于物理变化,而氧化钙与水反应生成氢氧化钙属于化学变化,反应的化学方程式为:CaO+H2O=Ca(OH)2;
【探究运用】碳酸钠与氢氧化钡在溶液反应生成碳酸钡白色沉淀和氢氧化钠;故填:Na2CO3+Ba(OH)2=BaCO3↓+2NaOH;
(1)步骤③中加入酚酞溶液后,若溶液E为红色,说明溶液呈碱性,原混合物中有氢氧化钡,碳酸钠与氢氧化钡反应生成碳酸钡沉淀和氢氧化钠.根据后面加入氯化钡后产生白色沉淀说明碳酸钠较多;则滤液E中除酚酞外还一定含有的溶质是NaOH、BaCl2;
根据现象可知,原混合物可能是氢氧化钡和碳酸钠组成的,也可能是硫酸钡、氢氧化钡和碳酸钠组成的;故填:Ba(OH)2、Na2CO3;BaSO4、Ba(OH)2、Na2CO3;
(2)白色沉淀可能是硫酸钡,也可能是碳酸钡,也可能是硫酸钡与碳酸钡的混合物,其中硫酸钡不与稀盐酸反应,而碳酸钡能与稀盐酸反应生成氯化钡、水和二氧化碳,故取少量滤渣B,加入过量的稀盐酸,若看到的现象是白色不溶物部分溶解,且有气泡产生,就足以说明原白色粉末的成分是BaSO4、Ba(OH)2、Na2CO3;
答案:
【现象分析】CaO+H2O=Ca(OH)2;
【探究运用】Na2CO3+Ba(OH)2=BaCO3↓+2NaOH;
(1)NaOH、BaCl2;Ba(OH)2、Na2CO3;BaSO4、Ba(OH)2、Na2CO3;
(2)BaSO4、Ba(OH)2、Na2CO3;
点评 本题考查了混合物组成的推断,完成此题,可以结合题干提供的实验现象根据物质的性质及反应的具体现象进行.


 优百分课时互动系列答案
优百分课时互动系列答案 开心蛙状元作业系列答案
开心蛙状元作业系列答案科目:初中化学 来源: 题型:多选题
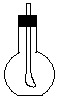 用如图装置做趣味实验:在用胶塞塞紧的烧瓶里充满某种气体(X),烧瓶内导管的一端事先已绑好了一个气球.拔开胶塞,迅速倒入另一种溶液(Y),再立即塞紧胶塞,振荡,此时可以看到气球逐渐膨胀的是( )
用如图装置做趣味实验:在用胶塞塞紧的烧瓶里充满某种气体(X),烧瓶内导管的一端事先已绑好了一个气球.拔开胶塞,迅速倒入另一种溶液(Y),再立即塞紧胶塞,振荡,此时可以看到气球逐渐膨胀的是( )| 选项 | X | Y |
| A | 氧气 | 澄清石灰水 |
| B | 氯化氢 | 氢氧化钾溶液 |
| C | 二氧化碳 | 盐酸溶液 |
| D | 二氧化碳 | 氢氧化钠溶液 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
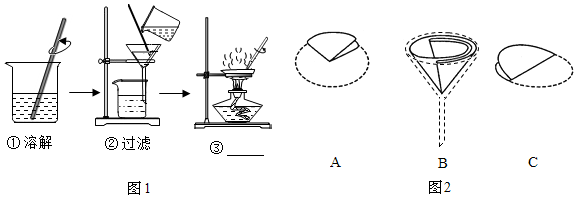
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
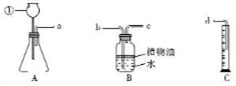 实验室用如图所示装置制取气体,并测定生成气体的体积.
实验室用如图所示装置制取气体,并测定生成气体的体积.查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
| 实验序号 | 实验操作 | 实验现象 | 实验结论 |
| 实验一 | 取少量滤液于试管中,向其中加入过量稀盐酸 | 无气泡产生 | 猜想一不成立 |
| 实验二 | 另取少量滤液于试管中,向其中滴入适量碳酸钠溶液 | 产生白色沉淀 | 猜想三成立,发生反应的化学方程式为 Ca(OH)2+Na2CO3=CaCO3+2NaOH |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
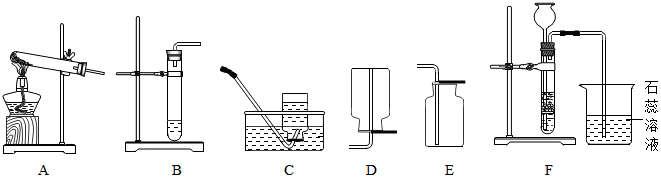
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com