
����Ŀ������г����������ҵ�г��õ�����Ư����
���� | �������� | �������� | Ư�� |
��ѧʽ | NaClO2 | ClO2 | Ca(ClO)2��CaCl2 |
(1)����Ư���У�Ca(ClO)2����___(�����)��
�ٻ���� �ڻ����� ��������
(2)ClO2����Ԫ�صĻ��ϼ�Ϊ___��
(3)�����е�����(��CaCl2)����Ԫ�ص���������������___��
(4)�������[Ca(ClO)2]��Ư�۵���Ч�ɷ֣�
�ٴ�������ڳ�ʪ�Ŀ����о��û����ɾ���Ư���Ե����ʴ�����(HClO)��������ˮ�İ�ɫ���壬��Ӧ�Ļ�ѧ����ʽ___���÷�Ӧ�Ļ���������___��
�ڹ�ҵʹ��Ư��ʱ������(4)�Тٵķ�Ӧԭ����ͨ������������___(�����)���������Ư��Ư���������⣮
A �������� B ϡ���� C �������� D �Ȼ��ƣ�
���𰸡��� +4 ClO2 Ca(ClO)2+H2O+CO2�TCaCO3��+2HClO ���ֽⷴӦ B
��������
(1)���û�ѧʽ��ʾ������һ���Ǵ�����Һ�������Ԫ��Ӧ�ǻ�������������������ڡ�
(2)��ClԪ�ػ��ϼ�Ϊx�����ݻ������и�Ԫ�صĻ��ϼ۵Ĵ�����Ϊ�㣬��x+(��2)��2��0 �� x��+4������+4��
(3)����������Ԫ������������![]() ��100����������������ԭ�Ӹ�����ȣ� ClO2����Է���������С��������Ԫ�ص���������������ClO2������ClO2��
��100����������������ԭ�Ӹ�����ȣ� ClO2����Է���������С��������Ԫ�ص���������������ClO2������ClO2��
(4) �ٸ��������غ㶨�ɿ�֪����Ӧ���ɵ�������ɫ������̼��ƣ��÷�ӦΪ������ơ�ˮ�Ͷ�����̼��Ӧ���ɴ������̼��Ƴ������ʷ�Ӧ�Ļ�ѧ����ʽдΪ��Ca(ClO)2+H2O+CO2=HCl+CaCO3����
������̼��ˮ��Ӧ����̼�ᣬ�÷�Ӧ�������ᷴӦ�������κ����ᣬ���ڸ��ֽⷴӦ������ֽⷴӦ��
����Ca(ClO)2�����ܷ�Ӧ���ɾ�Ư�����õ�HClO������Ӧѡ��ϡ���ᣬ����B��


 ��У����ϵ�д�
��У����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������25gʯ��ʯ��Ʒ���밴����Ҫ�����
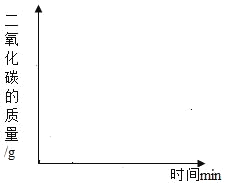
��1��25g��Ʒ��������ϡ���ᷴӦ�ų�8.8gCO2�����ʲ������ᣬ�Ҳ����ᷴӦ������������Ʒ�Ĵ��ȣ�CaCO3�������������Ƕ��٣�_____
��2������25g��Ʒƽ���ֳ����ݣ��ֱ�ӹ��ɿ�״�ͷ�ĩ״����������Ʒ�ֱ������ƿ�У�ͬʱ������ͬ�������ͬŨ�ȵ�����ϡ�����ַ�Ӧ������ͼ���ϻ�����״��Ʒ�ͷ�ĩ״��ϡ���ᷴӦ�ų�CO2������ʾ��ͼ��_____
��3������һ�������ĸ�ʯ��ʯ��Ʒ�������գ��й�����������Ӧʱ��ı仯�����ʾ��
ʱ��/min | t1 | t2 | t3 | t4 | t5 |
CO2����/g | 2.2 | 4.4 | 6.6 | 8.8 | 8.8 |
ʣ���������/g | 22.8 | 20.6 | m | 16.2 | 16.2 |
��m��_____��t3ʱʣ������г������⺬�е�������_____���ѧʽ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ȫ�����ؽ�����ũ�彨�裬��������·���Զ�װ����̫����·�ơ�̫����·�� ������̫���ܽ���������װ�á�̫����·����̫���ܵ�ذ塢���ء�LED·�Ƶ�ͷ�����������Կ������������ɡ�
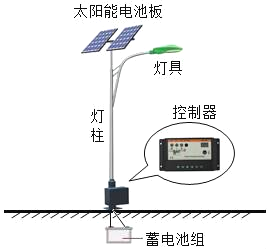
��1��̫���ܵ�ذ����Ҫ�����ǹ裬�赥������ʯ�ṹ���ƣ��ɹ赥�ʵ�������_____������ţ���ԭ��������������
��2�����ذ��콫_____��ת��Ϊ_____�ܴ���������
��3�����Ƶ������������ԭ����_____���û�ѧ����ʽ��ʾ��
��4����̫����·�Ƹ�����У�����Ҫ���������л��ϳɲ��ϵ���_____������ţ���
A ���ذ� B ���Ͻ���� C ���ϵ��� D ���ʷ�����˿��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������л�ѧ����й�˵����ȷ���ǣ�������
��H2��Na+��CO2��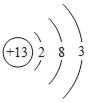 ��
��![]()
A. ���ɱ�ʾ2����ԭ��
B. �������ɱ�ʾ������
C. ����̼Ԫ�صĻ��ϼ�Ϊ+4��
D. ���С�+2����ʾ���Ȼ�þ��þ���Ӵ�������λ�������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����FeCl3��Һʴ��ͭ�������·��Ĺ����У���Һ����Ҫ����FeCl2��CuCl2����������Դ���յĹ�ҵ������ͼ��ʾ��
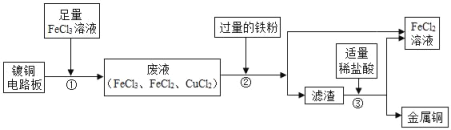
��1����������д����������Cu��FeCl3��Ӧ�Ļ�ѧ����ʽ��_____���������������ۺ������û���Ӧ�Ļ�ѧ����ʽΪ_____��
��2���������õ������ijɷ���_____���������IJ�����_____��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵���������
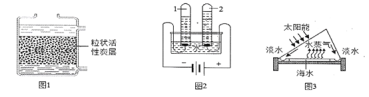
A. ͼ 1����̿����Ҫ��������������
B. ͼ 2���ˮʵ�飬�Թ�2�е�������п�ȼ��
C. ͼ 2ˮ�м�������������������Ƶ�ԭ������ǿˮ�ĵ����ԴӶ��ӿ췴Ӧ����
D. ͼ 3��ˮ�������䵭��ԭ�����ƽ̲��е�����ˮ�IJ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����1���ϸ���ָʾ����������:
ʵ�������õ���ҩƷ�����������ڼ�������ҵ����Ʒ���밴Ҫ����ա���ȡ200g�ϸ���˺��(ȥ����)������500mLˮ���м���200mLˮ���ڼ���ե֭�����飬��ʵ�����з���___________(����������)�е��á��ڼ���Ũ��Ϊ50%�ƾ����ݣ���ͥ����____________���棬������˫��ɴ�����ˣ����ã�ȡ�ϲ���Һ������ɫ���ϸ���ɫ����Һ��
(2)�����Na2O2����֬���д�������֬��ȼ����������֪:![]()
Na2O2��һ�ֵ���ɫ���壬����������CO2��H2O��HCl��������ʷ�Ӧ������O2��������N2��Ӧ��
ʵ��:���봿���������N2һ��ʱ�����ͨ����� CO2���۲쵽��֬����ȼ�ա���֤Na2O2����CO2��Ӧ���ͷų�����
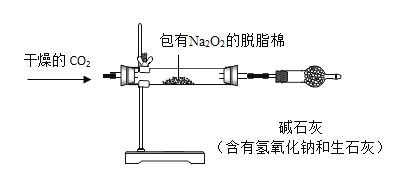
��ͨ�봿�������� N2��Ŀ����______________________________����ʯ�ҵ�������__________________��
�ڸ÷�Ӧ������һ���� A����Ӧ�Ļ�ѧ����ʽ��___________________����46g�Ƶ�����ȫ��Ӧ�ܲ���__________________g��A��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ѧ̽����ѧϰ��ѧ��Ҫ����Ч��ѧϰ������ijУ��ѧ��ȤС���ͬѧ����Ϊר�⣬��������ֻ�ѧ���ʽ���̽�����ܽἰӦ�ã���ش��й�����:
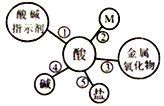
(1)��Ļ�ѧ���ʢ�һһ�������ָʾ�������á�����ʹ��ɫʯ����Һ��ɺ�ɫ������ʹ��ɫ��̪��Һ��ɫ��
(2)��Ļ�ѧ���ʢڣ�ͼ��M�����������������_______���ƽ���һ�ֳ�����Ʒ����ʵ�����У������̷��û�ͭð��ƽ���ۣ������û�ѧ�ķ������Լ���ijͬѧΪ�˲ⶨ��ͭ(ͭп�Ͻ�)��Ʒ�ijɷ֣���60gϡHCl�����μ��뵽ʢ��10g����Ʒ���ձ��У������������±�����û�ͭ��Ʒ�к�п����������Ϊ___________��
ʵ����� �������� | ��1�� | ��2�� | ��3�� |
����ϡ��������/ g | 20 | 20 | 20 |
��ַ�Ӧ��ʣ���������/g | 8.7 | 7.4 | 6.4 |
(3)��Ļ�ѧ���ʢ�һһ�������������ķ�Ӧ����������ڽ�����Ʒ�������ȡ�
(4)��Ļ�ѧ���ʢ�һһ����кͷ�Ӧ��
��У��ѧ��ȤС���ͬѧ�ص���������кͷ�Ӧ��Ϊ�������̽����С��ͬѧ���ձ��е�����������Һ�еμ�ϡ���ᣬһ����������˵μ����ָʾ����������ֹͣ�μ�ϡ���ᡣͬѧ�Ƿ�ʵ���ձ���Һ�к�����Щ����չ�������ۡ�
[�������]ʵ����ձ������ʺ�����Щ����?
[�������]����һ :������ֻ��Na2SO4
�����:���������Na2SO4��NaOH
������:���������____________________��
[��������] Na2SO4��Һ������
[ʵ��̽��]С��ͬѧ������µ�ʵ�鷽��
�������� | ʵ������ | ʵ����� | |
����һ | ȡ�����ձ��е���Һ�ڽྻ���Թ��У� ���뼸����ɫ��̪��Һ | ��̪�����ɫ | ����һ��ȷ ���������ȷ |
������ | ȡ�����ձ��е���Һ�ڽྻ���Թ��У� �μ�BaCl2��Һ | ���ְ�ɫ���� | ��������ȷ |
������ | ȡ�����ձ��е���Һ�ڽྻ���Թ��У��������ĺ�ɫCuO��ĩ���� | _________ | ��������ȷ |
[��������]ͬѧ�Ƕ�С�������ķ������ۺ���Ϊ:
�ٷ���һ����ȱ�ݣ��÷�������֤������һ����ȷ�ģ���ԭ����____________________��
�ڷ�����Ҳ����֤������������ȷ�ģ�������__________________________________��
��ͬѧ�Ǿ������ۣ�һ����Ϊ�������ܹ�֤������������ȷ�ģ������۳��˷����⣬���������ձ�����Һ�м�����ý�����̼���ε����ʽ���֤����
[ʵ�鷴˼]�ڷ�����ѧ��Ӧ���������ʳɷ�ʱ�����迼�Ƿ�Ӧ���������
[ѧ����]��ͼ��ʾ��С��ͬѧ�ڽ�����Һ�����Ե�ʵ��ʱ�����缫���˲���ϡH2SO4��Һ�У��պϿ��أ�С�����������⣬Ȼ�������ϡH2SO4�м���Ba(OH)2��Һ�����������Ʋ�С���ݵķ������Ϊ__________________��������Ӧ�Ļ�ѧ����ʽ��___________��
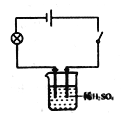
(5)��Ļ�ѧ���ʢ�һһ�����εķ�Ӧ
������ͼ��ʾװ������֤CO2��������ʣ�Ҫ֤��CO2��NaOH��Һ�ܹ�������Ӧ�����ȼ�����������Һ���ټ����ᣬ����ı仯��_____________��
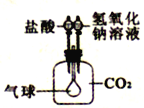
[��������]�ڻ�ѧʵ���У���ͨ����֤��Ӧ��������Ĵ��ڣ�����֤ij��ѧ��Ӧ�ķ�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij����С��ͬѧ��ͼ��װ��(�̶�װ��δ����)�ⶨ�������ʵ�þ����þ���ʵ���������(��������Ӵ�����������)��ʵ��������£�
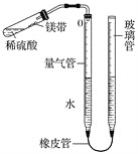
��ȡһ��þ����Ʒ��ȷ�Ƶ�������Ϊ0.030 g��
������������װˮ�����ڿ̶���0����λ�ã���ͼ��ʾ��(δװҩƷ)װ���������
��_________________________��
�����Թ��м���������ϡ���ᣬ����б�Թܣ�����ˮʪ���þ��С�������Թܱ��ϣ�������Ƥ����
�ݵ���������Һ�棬ʹ���ߵ�Һ�汣��ͬһˮƽ����¼��������Һ��λ�ã�
�ް��Թܵײ���Ϊ̧�ߣ�ʹþ����ϡ����Ӵ���ȫ��Ӧ��
�ߴ���ȴ�����º��ٴμ�¼��������Һ��λ�ã�
����������������ӵ��������Ϊ23.96 mL��
��֪��ͬ��ͬѹ�£���ͬ�����Ϻ�������ڻ��ǰ���������֮�͡�
��ش��������⣺
(1)д��þ��ϡ���ᷴӦ�Ļ�ѧ����ʽ��____________________��
(2)�ܷ���������ƽ����0.030 gþ����Ʒ________(������������������)��
(3)��������_________________________��
(4)ʵ����̢����ٴμ�¼�����ܵ�Һ��λ��ʱ���Թ��������������Ƿ��Ӱ��ʵ�����ս��________(����������������)��������_______________________��
(5)��ʵ�ʲ�����������������ֵ���ƫ������ܵ�ԭ����________________________��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com