
【题目】已知碳的相对原子质量为12,氧的相对原子质量为16。
(1)已知一个二氧化碳分子是由一个碳原子和两个氧原子构成。则每个二氧化碳分子中共有______个原子核,_______个质子,_______个中子;
(2)钠的相对原子质量为23,核内有11个质子,则核内有_____个中子,核外有____电子。
(3)铁原子的质子数为26,中子数比质子数多4个,该原子中微粒总数为_____个;
(4)Ax-的核外电子数为y,其相对原子质量为m,则其核内中子数为___________。
【答案】3 22 22 12 11 56 m+x-y
【解析】
(1)已知一个二氧化碳分子是由一个碳原子和两个氧原子构成。每个原子中有一个原子核,则每个二氧化碳分子中共有1+2=3个原子核;一个二氧化碳分子中质子总数等于1个碳原子和2个氧原子的质子数之和,对于原子,原子序数=核电荷数=核内质子数=核外电子数,故1个碳原子核内有6个质子,1个氧原子核内有8个质子,则一个二氧化碳分子中含有6+8×2=22个质子;一个二氧化碳分子中中子数总数等于1个碳原子和2个氧原子的中子数之和,相对原子质量![]() 质子数+中子数,已知碳的相对原子质量为12,质子数为6,则其中子数=12-6=6,氧的相对原子质量为16,质子数=8,则中子数=8,一个二氧化碳分子中有6+8×2=22个中子;
质子数+中子数,已知碳的相对原子质量为12,质子数为6,则其中子数=12-6=6,氧的相对原子质量为16,质子数=8,则中子数=8,一个二氧化碳分子中有6+8×2=22个中子;
(2)钠相对原子质量为23,核内质子数=原子序数=11,核内有11个质子,根据相对原子质量![]() 质子数+中子数,则核内有:23-11=12个中子;核内质子数=核外电子数,钠核外有11个电子;
质子数+中子数,则核内有:23-11=12个中子;核内质子数=核外电子数,钠核外有11个电子;
(3)铁原子质子数为26,中子数比质子数多4个,则中子数=26+4=30,该原子核中微粒总数=质子数+中子数=26+30=56;
(4)Ax-是A原子得到x个电子形成的,Ax-的核外电子数为y,则A原子的核外电子数为y-x,根据原子中核电荷数=核内质子数=核外电子数,则该原子的核内质子数为y-x;其相对原子质量为m,根据相对原子质量![]() 质子数+中子数,则核内中子数为m-(y-x)=m+x-y。
质子数+中子数,则核内中子数为m-(y-x)=m+x-y。


 开心蛙状元测试卷系列答案
开心蛙状元测试卷系列答案科目:初中化学 来源: 题型:
【题目】化学课堂上要学习碱的化学性质,老师让两位同学和他共同做实验,要求两位同学分别向澄清石灰水和氢氧化钠溶液中吹气,如图①②所示,老师告诉同学们,呼出的气体中只有二氧化碳有可能与澄清石灰水和氢氧化钠溶液反应。
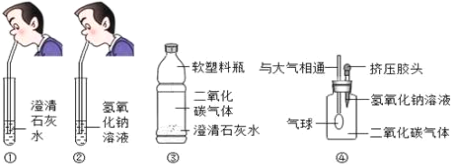
同学们在吹气后观察到①中澄清石灰水变浑浊,②中氢氧化钠溶液无明显现象。观察实验现象后老师问,通过实验现象的观察,检验二氧化碳气体应该使用________,针对②中的情况,师生共同开始探究之旅。
(提出问题)二氧化碳通入氢氧化钠溶液中无明显现象,两者是否发生了化学反应?
(猜想假设)猜想A:两者发生了化学反应;猜想B:两者没有发生化学反应。
(实验探究)
Ⅰ:小明设计了如图所示的③、④两个实验。
实验现象:③中的软塑料瓶________________,④中气球膨胀。
II:小亮认为小明的实验是可行的,其共同原理是二氧化碳和氢氧化钠溶液反应,使容器内压强降低,小光同学却对此提出了质疑,他认为小明的实验不严谨,若仍利用该装置,需要补做的对比实验是___________。
III:小光设计的是通过检验生成物来验证猜想,请帮他填写实验报告:
实验步骤 | 实验现象 | 实验结论 |
取④实验后的溶液少许,再向其中加入____________。 | _________ | 验证了二氧化碳和氢氧化钠溶液反应。 |
(实验结论)二氧化碳和氢氧化钠溶液发生了化学反应。
(反思拓展)实验②中反应后所得溶液中溶质成分:猜想(1):只有碳酸钠;猜想(2):__________。
(数据处理)
小明将实验③中浑浊的液体进行_______(填操作名称)、洗涤、烘干,称量所得固体质量为1.0g。试计算:实验③中参加反应的二氧化碳的质量为____________克?(列式计算)
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】依据下图有关信息判断,下列说法正确的是
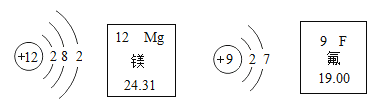
A.在元素周期表中,镁元素与氟元素属于同一周期
B.镁离子与氟离子核外电子数相等
C.镁原子与氟原子形成的化合物的化学式为Mg2F
D.氟原子的核内有9个中子
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图为一氧化碳还原氧化铁的“微型”实验装置,已知: ,下列说法错误的是
,下列说法错误的是
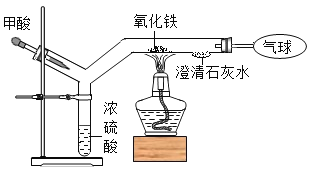
A.实验中所需CO可现制现用
B.此装置可节约用品,污染小
C.可以观察到固体由黑色变为红色
D.用气球收集尾气可减少一氧化碳对大气的污染
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】化学是认识、改造和应用物质的科学。从海水中提取镁、制“碱”,都体现了人类改造物质的智慧。结合下列流程图(部分操作和条件已略去),请回答相关问题:
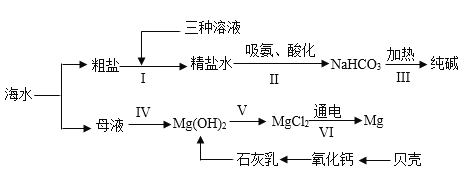
(1)提纯物质常用转化的方法,就是将杂质转化为沉淀或气体而除去。粗盐中 含有氯化镁、硫酸钠、氯化钙等可溶性杂质,通过步骤I,再利用过滤操作进行除杂。步骤I加入下列三种溶液的先后顺序为____(填字母序号)。
a 稍过量的Na2CO3溶液
b 稍过量的BaCl2溶液
c 稍过量的NaOH溶液
(2)母液中有MgC12,却经历了步骤IV、V的转化过程,其目的是__________。
(3)步骤II中先向饱和食盐水中通入氨气,有利于二氧化碳的吸收,写出该反应的化学方程式________;步骤VI反应的化学方程式__________。
(4)化学变化是改造物质的重要途径。上述流程 图中没有涉及的基本反应类型是_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】化肥对提高粮食产量具有重要的作用。尿素[化学式:CO(NH2)2]是一种常用的化肥,工业上生产尿素的反应的微观示意图如下:
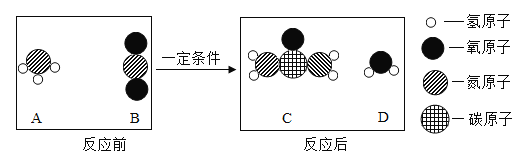
(1)四种物质中属于氧化物的有___(填化学式)。
(2)工业上生产尿素的生产尿素的反应中A、B的质量比为_________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下图一是非金属元素形成微粒的结构示意图。该非金属单质可以用多种方法制得,下图二为其中一种制法的反应的微观示意图。
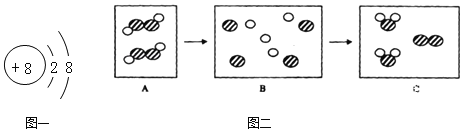
请根据以上信息回答问题:
(1)该非金属元素的原子最外层电子数=_____;图一所示的微粒的符号为_____.
(2)写出与图二相符的反应的化学方程式_____.
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】专家提示在日常防控新型冠状病毒中“84”消毒液可以使病毒灭活。
(1)其有效成分NaClO中氯元素的化合价为____,所含的阳离子为____(写离子符号)。
(2)“84”消毒液的消毒原理为2NaClO+CO2+X═Na2CO3+2HClO,生成的HClO(次氯酸)具有较强的杀菌作用。化学方程式中X的化学式为____。
(3)“84”消毒液有一定的刺激性与腐蚀性,必须稀释以后才能使用。将50g含NaClO 5%的“84”消毒液稀释至1%,需向原溶液中加入水的质量为_________ 。
(4)酒精(C2H5OH)和过氧乙酸(CH3COOOH)也均是能有效灭活新冠病毒的消毒剂,二者分别在氧气中完全燃烧的产物是相同的,从物质组成的角度解释其原因是___________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】在一个密闭装置中放入甲、乙、丙、丁四种物质,在一定条件下发生化学反应,反应前后各物质的质量变化如图所示,下列分析正确的是( )
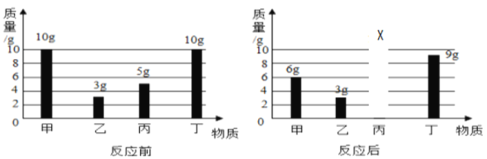
A.反应的基本类型为分解反应B.乙物质一定是催化剂
C.参加反应的甲、丁的质量之比为4:1D.反应后丙的质量X为8g
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com