
 已知A、B、C、D、E、F、G、H、M、N均为初中化学中常见的物质,其中A、C、D、M、F为氧化物,组成A与C的元素种类相同;H为可溶性碱;固体X在B中充分燃烧可生成无色气体D;E为常用建筑材料的主要成分.各物质之间的相互关系如图所示(部分反应条件和生成物已省略)
已知A、B、C、D、E、F、G、H、M、N均为初中化学中常见的物质,其中A、C、D、M、F为氧化物,组成A与C的元素种类相同;H为可溶性碱;固体X在B中充分燃烧可生成无色气体D;E为常用建筑材料的主要成分.各物质之间的相互关系如图所示(部分反应条件和生成物已省略)分析 根据A、B、C、D、E、F、G、H、M、N均为初中化学中常见的物质,A、C、D、M、F为氧化物,固体X在B中充分燃烧可生成无色气体D,所以B是氧气,组成A与C的元素种类相同,A会生成C和氧气,所以A是过氧化氢溶液,C是水,E为常用建筑材料的主要成分,D和G会生成E,所以E是碳酸钙,D是二氧化碳,X就是木炭,碳酸钙高温分解会生成氧化钙和二氧化碳,所以F是氧化钙,氧化钙和水会生成氢氧化钙,所以G是氢氧化钙,H为可溶性碱,二氧化碳和H生成的N会与氢氧化钙反应,所以H是氢氧化钠,N是碳酸钠,然后将推出的物质进行验证即可.
解答 解:(1)A、B、C、D、E、F、G、H、M、N均为初中化学中常见的物质,A、C、D、M、F为氧化物,固体X在B中充分燃烧可生成无色气体D,所以B是氧气,组成A与C的元素种类相同,A会生成C和氧气,所以A是过氧化氢溶液,C是水,E为常用建筑材料的主要成分,D和G会生成E,所以E是碳酸钙,D是二氧化碳,X就是木炭,碳酸钙高温分解会生成氧化钙和二氧化碳,所以F是氧化钙,氧化钙和水会生成氢氧化钙,所以G是氢氧化钙,H为可溶性碱,二氧化碳和H生成的N会与氢氧化钙反应,所以H是氢氧化钠,N是碳酸钠,经过验证,推导正确,所以A是H2O2;
(2)G和N的反应是碳酸钠和氢氧化钙反应生成碳酸钙沉淀和氢氧化钠,化学方程式为:Ca(OH)2+Na2CO3=CaCO3↓+2NaOH;
(3)通过推导可知,F是氧化钙,俗称生石灰,氧化钙和水反应生成氢氧化钙,放出热量;
(4)氧化钙和水生成氢氧化钙的反应属于化合反应,碳酸钙高温生成氧化钙和二氧化碳的反应是分解反应,碳酸钠和氢氧化钙生成碳酸钙沉淀和氢氧化钠的反应属于复分解反应,没有涉及到的基本反应类型为置换反应.
故答案为:(1)H2O2;
(2)Ca(OH)2+Na2CO3=CaCO3↓+2NaOH;
(3)生石灰,放出大量热;
(4)置换反应.
点评 在解此类题时,首先将题中有特征的物质推出,然后结合推出的物质和题中的转化关系推导剩余的物质,最后将推出的各种物质代入转化关系中进行验证即可.


科目:初中化学 来源: 题型:填空题
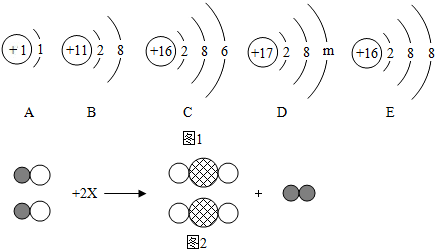
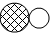 .
.查看答案和解析>>
科目:初中化学 来源: 题型:填空题

查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | ①②⑥ | B. | ④⑤⑥ | C. | ①⑤⑥ | D. | ①②③ |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 原子核是由质子和中子构成的,所以所有原子的原子核都含有质子和中子 | |
| B. | 常见的铁合金有生铁和钢,其中钢的含碳量比生铁的高 | |
| C. | 石墨具有滑腻感,因此石墨可以做铅笔芯 | |
| D. | 喝了汽水会打嗝,因为温度升高,气体的溶解度减小 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 稀有气体包括氦、氖、氩、氪、氙和氡六种气体,约占空气体积的0.94%.常温常压下,稀有气体都是无色无味,微溶于水,且熔点和沸点都很低.由于稀有气体元素原子的最外层电子排布是稳定结构,所以它们的化学性质非常稳定,但在一定条件下,氙气(Xe)可与氟气(F2)发生反应,生成四氟化氙(XeF4).工业上,制取稀有气体是通过将液态空气蒸馏,得到稀有气体的混合物,再用活性炭低温吸附法,将稀有气体分离开来.在焊接精密零件或镁、铝等活泼金属时,常用氩作保护气.氦气是除了氢气外的最轻气体,可以代替氢气应用在飞艇中,不会着火和发生爆炸.利用稀有气体通电时发出色彩绚丽的光芒,可制成霓虹灯.
稀有气体包括氦、氖、氩、氪、氙和氡六种气体,约占空气体积的0.94%.常温常压下,稀有气体都是无色无味,微溶于水,且熔点和沸点都很低.由于稀有气体元素原子的最外层电子排布是稳定结构,所以它们的化学性质非常稳定,但在一定条件下,氙气(Xe)可与氟气(F2)发生反应,生成四氟化氙(XeF4).工业上,制取稀有气体是通过将液态空气蒸馏,得到稀有气体的混合物,再用活性炭低温吸附法,将稀有气体分离开来.在焊接精密零件或镁、铝等活泼金属时,常用氩作保护气.氦气是除了氢气外的最轻气体,可以代替氢气应用在飞艇中,不会着火和发生爆炸.利用稀有气体通电时发出色彩绚丽的光芒,可制成霓虹灯.查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 同学们学习碱的化学性质时,进行了如图所示的实验.
同学们学习碱的化学性质时,进行了如图所示的实验.查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | ①②③ | B. | ①②⑥ | C. | ①③④ | D. | ③⑤⑥ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com