
分析 首先根据反应原理找出反应物、生成物、反应条件,根据化学方程式的书写方法、步骤(写、配、注、等)进行书写;再根据反应特征确定反应类型.
解答 解:(1)氢氧化镁和胃酸中的盐酸反应生成氯化镁和水,反应的化学方程式为:Mg(OH)2+2HCl═MgCl2+2H2O;
(2)酒精燃烧生成二氧化碳和水,反应的化学方程式为:C2H5OH+3O2$\frac{\underline{\;点燃\;}}{\;}$2CO2+3H2O;
(3)工业上用一氧化碳还原氧化铁炼铁,主要是利用CO的还原性,在高温下和氧化铁反应生成铁和二氧化碳,反应的化学方程式为Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2.
故答案为:(1)Mg(OH)2+2HCl═MgCl2+2H2O;(2)C2H5OH+3O2$\frac{\underline{\;点燃\;}}{\;}$2CO2+3H2O;(3)Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2.
点评 本题难度不大,考查学生根据反应原理书写化学方程式、判定反应类型的能力,掌握化学方程式的书写方法(写、配、注、等)、四种基本反应类型的特征即可正确解答本题.


科目:初中化学 来源: 题型:选择题
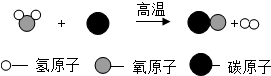 为减少污染、提高煤的利用率,可将煤转化为可燃性气体,其微观示意图如图所示,下列说法错误的是( )
为减少污染、提高煤的利用率,可将煤转化为可燃性气体,其微观示意图如图所示,下列说法错误的是( )| A. | 原子是化学变化中的最小粒子 | |
| B. | 保持水的化学性质的最小粒子为水分子 | |
| C. | 反应前后元素的种类不变 | |
| D. | 反应前后分子的种类和数目保持不变 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
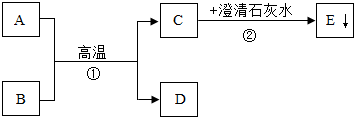
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | CH4 H2 CO | B. | CH4 CO H2 | ||
| C. | H2 CH4 CO | D. | CO CH4 H2 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
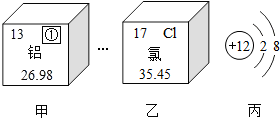 请根据原子结构知识和如图信息填空:
请根据原子结构知识和如图信息填空:查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 试管编号 | 1 | 2 | 3 | 4 | 5 |
| KIO3溶液滴数 | 30 | 25 | 20 | 15 | 10 |
| 测试液滴数 | 10 | 10 | 10 | 10 | 10 |
| 蒸馏水滴数 | 0 | 5 | 10 | 15 | 20 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 合金是由两种或两种以上金属熔合而成的具有金属特性的物质 | |
| B. | 在日常生活中,大量使用的常常不是纯金属,而是它们的合金 | |
| C. | 所有金属都能与稀硫酸反应生成氢气 | |
| D. | 铜的化学性质不活泼,所以铜制品不会生锈 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com