
| A. | 稀有气体在通常条件下几乎不与任何物质发生反应,化学性质比较稳定 | |
| B. | 铁制品锈蚀主要是铁与空气汇总的氧气、水蒸气发生化学反应的结果 | |
| C. | 溶液具有均一性和稳定性,是因为构成溶质的粒子均匀分散到溶剂分子中 | |
| D. | 用碘化钾溶液检验食品中是否含有淀粉 |
分析 根据已有的知识进行分析,稀有气体化学性质比较稳定,铁能与氧气、水发生缓慢氧化生成铁锈,各种粒子都不停的运动,碘单质常用来检验淀粉的存在进行分析.
解答 解:A、稀有气体在通常条件下几乎不与任何物质发生反应,化学性质比较稳定,故A正确;
B、铁制品锈蚀主要是铁与空气中氧气、水蒸气发生化学反应的结果,故B正确;
C、根据微观粒子的性质可知,溶液具有均一性和稳定性,是因为构成溶质的粒子均匀分散到溶剂分子中,故C正确;
D、碘单质常用来检验淀粉的存在,故D错误.
故选:D.
点评 本题难度不大,物质的性质决定物质的用途,掌握常见物质的性质和用途、铁生锈的原理以及微观粒子的性质等是正确解答此类题的关键.


科目:初中化学 来源: 题型:解答题
| 实验操作 | 测定结果 | 白色固体成分 |
| 用pH试纸测定反应后溶液的酸碱度,操作方法是 用玻璃棒蘸取溶液滴到pH试纸上,把试纸显示的颜色与标准比色卡比较 | pH>7 | |
| pH=7 | CaCl2 |
| OH- | Cl- | SO42- | CO32- | |
| H+ | 溶、挥 | 溶 | 溶、挥 | |
| Ba2+ | 溶 | 溶 | 不溶 | 不溶 |
| Ca2+ | 微溶 | 溶 | 微溶 | 不溶 |
| Mg2+ | 不溶 | 溶 | 溶 | 微溶 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题

 表示:氧原子
表示:氧原子 表示;氢原子
表示;氢原子  表示:氯原子
表示:氯原子查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
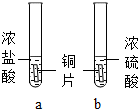 化学课上探究金属的化学性质时,同学们发现铜与稀盐酸、稀硫酸在常温或短时间加热的条件下均不反应.那么,铜与浓盐酸、浓硫酸能否发生反应呢?兴趣小组进行如下探究.
化学课上探究金属的化学性质时,同学们发现铜与稀盐酸、稀硫酸在常温或短时间加热的条件下均不反应.那么,铜与浓盐酸、浓硫酸能否发生反应呢?兴趣小组进行如下探究.查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com