
分析 根据化学方程式和元素的相对原子质量可以得出反应物和生成物的质量比,然后根据已知条件和质量守恒定律,即可计算出其它各项的质量.
解答 解:铁、氧气、四氧化三铁的质量比为(3×56):(2×32):232=168:64:232.
设8.4g铁需质量为x的氧气恰好完全反应,生成Fe3O4的质量为y,则
3Fe+2O2$\frac{\underline{\;点燃\;}}{\;}$Fe3O4
168 64 232
8.4g x y
$\frac{168}{64}$=$\frac{8.4g}{x}$,x=3.2g
$\frac{168}{232}$=$\frac{8.4g}{y}$,y=11.6g
设如果要制取23.2g Fe3O4,需Fe 的质量为m,需O2 的质量为n,则
3Fe+2O2$\frac{\underline{\;点燃\;}}{\;}$Fe3O4
168 64 232
m n 23.2g
$\frac{168}{232}$=$\frac{m}{23.2g}$,m=16.8g
$\frac{64}{232}$=$\frac{n}{23.2g}$,n=6.4g
故答案为:168﹕64﹕232;3.2;11.6;16.8; 6.4.
点评 本题主要考查学生运用化学方程式和元素的相对原子质量以及质量守恒定律进行计算的能力.


 一本好题口算题卡系列答案
一本好题口算题卡系列答案科目:初中化学 来源: 题型:选择题
| A. | ①⑥ | B. | ③⑤ | C. | ②③⑤ | D. | ②③④ |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
 ;
;查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
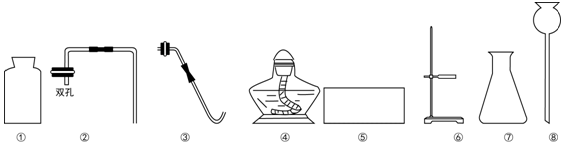
查看答案和解析>>
科目:初中化学 来源: 题型:推断题
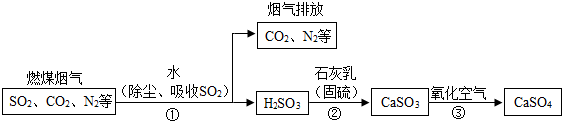
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com