
| A. | 该反应的化学方程式中,X的化学计量数是12 | |
| B. | X由三种元素组成,其中一定含有氯元素 | |
| C. | X中所含元素的质量比为l:35.5 | |
| D. | 该实验发生装置与实验室用高锰酸钾制氧气的发生装置相同 |
 浙大优学小学年级衔接导与练浙江大学出版社系列答案
浙大优学小学年级衔接导与练浙江大学出版社系列答案 小学暑假作业东南大学出版社系列答案
小学暑假作业东南大学出版社系列答案 津桥教育暑假拔高衔接广东人民出版社系列答案
津桥教育暑假拔高衔接广东人民出版社系列答案 波波熊暑假作业江西人民出版社系列答案
波波熊暑假作业江西人民出版社系列答案科目:初中化学 来源: 题型:填空题

查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 酸碱发生中和反应生成盐和水,所以生成盐和水的反应一定是中和反应 | |
| B. | 酸溶液中都含有氢离子,所以含有氢元素的物质一定是酸 | |
| C. | 有机物都含有碳元素,所以含有碳元素的化合物一定是有机物 | |
| D. | 化合物是由不同元素组成的纯净物,所以只含一种元素的物质一定不是化合物 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
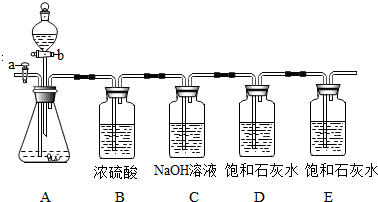
 某教师设计的创新实验装置图如图,请完成下列探究:
某教师设计的创新实验装置图如图,请完成下列探究:查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| 选项 | 物质(括号内为杂质) | 试剂 | 操作方法 |
| A | Cu(CuO) | 足量稀硫酸 | 过滤、洗涤、干燥 |
| B | NaCl(KNO3) | 水 | 溶解、降温结晶、过滤 |
| C | NaCl(MgCl2) | 过量NaOH溶液 | 过滤、蒸发结晶 |
| D | CO2(CO) | 足量O2 | 点燃 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 90% | B. | 95% | C. | 80% | D. | 70% |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com