
【题目】根据以下题图回答有关问题:
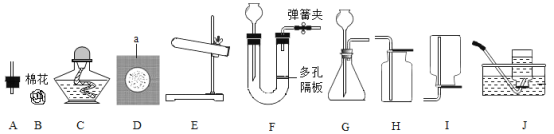
(1)仪器a的名称是_____________。
(2)实验室用KMnO4制备O2的发生装置应选用的装置仪器是____________(填序号,下同),反应的化学方程式是_____________。若用装置J收集氧气,当气体收集完毕时,应先___________,后____________。
(3)制备氢气能使反应随时发生或停止应选用的装置是____________,发生反应的化学方程式为__________,收集装置应选_____________。
(4)实验室制备Cl2的原理是:![]() ,制备Cl2应选用的装置是(夹持装置略去)___________,Cl2能溶于水,密度比空气大,收集Cl2应选用的装置是____________。
,制备Cl2应选用的装置是(夹持装置略去)___________,Cl2能溶于水,密度比空气大,收集Cl2应选用的装置是____________。
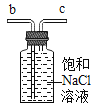
(5)若用如图装置收集Cl2,气体应从___________口进入。
【答案】石棉网 ABCE ![]() 移出导管 熄灭酒精灯 F
移出导管 熄灭酒精灯 F ![]() I或J CDG H c
I或J CDG H c
【解析】
(1)仪器a的名称是石棉网;
(2)如果用高锰酸钾制氧气就需要加热,应选固-固加热型发生装置,所以选用的装置用品是ABCE;高锰酸钾受热分解生成锰酸钾和二氧化锰和氧气,其反应的化学方程式为:![]() ;用排水法收集氧气时,为了防止水倒流,使试管炸裂,实验结束应先移出导管,后熄灭酒精灯;
;用排水法收集氧气时,为了防止水倒流,使试管炸裂,实验结束应先移出导管,后熄灭酒精灯;
(3)实验室是用锌粒和稀硫酸在常温下反应制氢气的,应选固-液、不加热型发生装置,含长颈漏斗及隔板的发生装置可以起到随开随用、随关随停的作用,所以制备氢气能使反应随时发生或停止应选用的装置是F;锌和硫酸反应生成硫酸锌和氢气,其反应的化学方程式为:![]() ;氢气难溶于水,密度比空气的密度小,因此可以用排水法和向下排空气法收集,可用I或J收集;
;氢气难溶于水,密度比空气的密度小,因此可以用排水法和向下排空气法收集,可用I或J收集;
(4)由Cl2的制备原理可知,发生装置为:固-液、加热型,所以制备Cl2应选用的装置是: CDG; Cl2能溶于水,密度比空气大,收集Cl2应用向上排空气法,选用的装置是H;
(5)若用图2装置收集Cl2,气体应从短管进入,因为氯气的密度比液体小。


科目:初中化学 来源: 题型:
【题目】某化学兴趣小组,为了测定铜锌合金样品中锌的含量,称取样品20克于烧杯中,向其中加入50克稀硫酸至恰好完全反应,反应后烧杯中物质的总质量为69.8克,求:
(1)样品中锌的质量分数?
(2)稀硫酸溶质的质量分数?
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】预防“新冠肺炎”要经常杀菌消毒。过氧乙酸![]() 化学式为
化学式为![]() )是一种广谱、高效杀菌消毒剂,下列说法正确的是()
)是一种广谱、高效杀菌消毒剂,下列说法正确的是()
A.过氧乙酸是由碳元素,氢元素和氧元素组成的
B.过氧乙酸分子中含有氧气
C.过氧乙酸中碳、氢、氧元素的原子个数是6:1:12
D.过氧乙酸分子是由碳、氢、氧三种原子组成
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】A、B、 C、D、E、F、G、H分别是硝酸银溶液、碳酸钠溶液、稀盐酸、氢氧化钙溶液、硫酸铜溶液、铁丝、氧化铁和水八种物质中的一种;用连线表示物质能反应,用箭头表示物质可以转化。试回答下列问题: (不考虑氢氧化银)
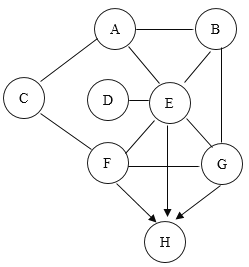
(1)在圆内写出各物质(或溶质)的化学式________。
(2) E与D反应的化学方程式:__________________。
(3)B与G反应的实验现象:__________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】能正确反映对应变化关系的图像是
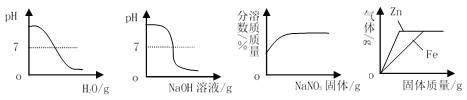
A. 稀释NaOH溶液
B. 向一定量的稀硫酸中滴加氢氧化钠溶液至过量
C. 一定温度下,向不饱和硝酸钠溶液中不断加入硝酸钠固体,充分搅拌
D. 分别向同质量、同质量分数的稀盐酸中不断加入锌片和铁片
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某化学兴趣小组为了测定实验室用大理石和稀盐酸制备CO2后溶液的组成,取50g反应后的溶液,向其中加入10%的Na2CO3溶液,先出现气泡,后出现白色沉淀。反应过程中加入Na2CO3溶液质量与生成的气体及沉淀质量关系如图。
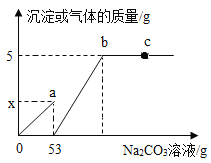
(1)生成沉淀的质量是 g。
(2)50g溶液中CaCl2的质量分数是 ?(写出计算过程)
(3)X= 。
(4)C点对应的溶液的溶质是(填化学式) 。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】乙基麦芽酚(C7H8Ox)是一种安全无毒的理想食品添加剂,是烟草、食品、饮料、香精等良好的香味增效剂,对食品的香味改善具有显著效果,且能延长食品储存期。请计算:
(1)乙基麦芽酚的相对分子质量为140,则x的数值为_________。
(2)乙基麦芽酚中碳、氢、氧三种元素的质量比为_________。
(3)5.6g的乙基麦芽酚中含有_______g氢元素。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】在一个密闭容器中放入W、G、H、P四种物质,在一定条件下发生化学反应,一段时间后,测得有关数据如表,关于此反应的认识不正确的是( )
物质 | W | G | H | P |
反应前质量/g | 20 | 2 | 1 | 37 |
反应后质量/g | a | 32 | 1 | 12 |
A.a=15
B.H可能是该反应的催化剂
C.若W和P的化学式量之比为1:5,则W和P的化学计量数之比为1:1
D.在反应中,G、P的质量比为5:6
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某化学兴趣小组进行了下列探究实验:
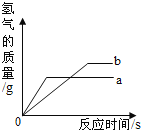
(1)将等质量且表面积相同的镁片和铝片分别与等质量且溶质质量分数相同的稀硫酸反应。
①请描述稀释浓硫酸的操作方法_______。
②实验前要打磨铝片,原因是什么?_________
③若实验过程中产生氢气的质量与时间的关系如图。b曲线代表的反应的化学方程式为_____________;若充分反应后有一种金属剩余,则剩余的金属一定是___________(填化学式)。
(2)现有一包固体粉末可能含有Na2CO3、CuSO4、BaCl2 、NaOH中的一种或几种,为了探究它的成分,进行了如下实验:
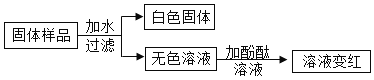
①推断粉末中一定含有的物质有_________________________。
②为了确定可能还有的物质,请设计实验证明(简要写出实验步骤、现象和结论) __________。
(3)取氯酸钾和二氧化锰的混合物共16 g,充分加热后得到11.2 g固体物质。
①二氧化锰在反应中起到的作用是_______________________。
②请计算原固体混合物中氯酸钾的质量______。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com