
��6�֣�KNO3��NaCl��Һ������������������ʮ����Ҫ�����á���ͼ�����ǵ��ܽ�����ߣ��±��������ڲ�ͬ�¶�ʱ���ܽ�ȡ�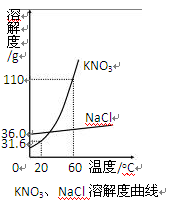

��1���������������ܽ�ȵı仯���¶�Ӱ���С����________��
��2���������Һ�е�������________��
��3��30��ʱ��KNO3���ܽ����________g��
��4��ũҵ�����������ʵ���������Ϊ10% ~ 20%��NaCl��Һ��ѡ�֡���ɴ���Һ��������ȷ�IJ���˳���ǣ�����ţ� ��
���ܽ� �ڳ��� �ۼ��� ����ȡ
��5��ijͬѧ������������ʵ�顣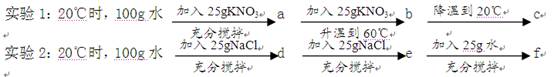
�ж�a��f��Ӧ����Һ�У�Ϊ������Һ���� ��
��ʵ��1��2��֪��ʹ��������Һת��Ϊ������Һ�ķ����� ��
 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
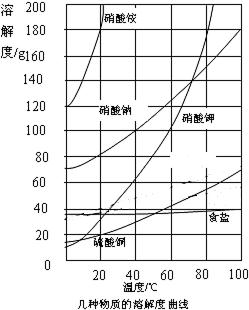 25����ͼ�Ǽ��ֹ������ʵ��ܽ�����ߣ������ͼ�ش��������⣺
25����ͼ�Ǽ��ֹ������ʵ��ܽ�����ߣ������ͼ�ش��������⣺�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
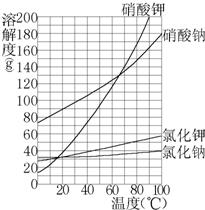 25����ͼΪNaNO3��KNO3��NaCl����KCl ���ܽ�����ߣ���ش�������������⣺
25����ͼΪNaNO3��KNO3��NaCl����KCl ���ܽ�����ߣ���ش�������������⣺�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| �¶�/�� | 0 | 10 | 20 | 30 | 40 | 50 | 60 | 70 | 80 | 90 | 100 | |
| �ܽ�� /g |
NaCl | 35.7 | 35.8 | 36 | 36.3 | 36.6 | 37 | 37.3 | 37.8 | 38.4 | 39 | 39.8 |
| KNO3 | 13.3 | 20.9 | 32 | 45.8 | 64 | 85.5 | 110 | 138 | 169 | 202 | 246 | |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com