
25℃时,向20.0mL质量分数为30%的盐酸中滴加氢氧化钠溶液,溶液的pH与所加氢氧化钠溶液的体积如图所示,下列有关叙述正确的是
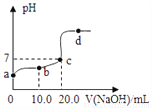
A. d点对应的溶液中溶质是NaCl和NaOH
B. 所用氢氧化钠溶液的质量分数一定为30%
C. 向b点对应的溶液中滴加石蕊溶液,溶液呈无色
D. b、d点对应溶液的pH:b>d
A 【解析】A. d点表示氢氧化钠过量,对应的溶液中溶质NaCl和NaOH,正确;B. 向20.0mL质量分数为30%的盐酸中滴加氢氧化钠溶液,由图可知刚好完全反应时,需要氢氧化钠溶液20.0mL,NaOH +HCl == NaCl + H2O,由方程式可知氢氧化钠和氯化氢的质量比为40:36.5,故所用氢氧化钠溶液的质量分数一定大于30%,错误;C. b点氢氧化钠不足,盐酸有剩余,对应的溶... 暑假接力赛新疆青少年出版社系列答案
暑假接力赛新疆青少年出版社系列答案科目:初中化学 来源:河南省信阳市2018届九年级下学期最后一次模拟考试化学试卷 题型:流程题
为探究工业废水的综合利用,某化学小组在实验室中完成了以下实验。
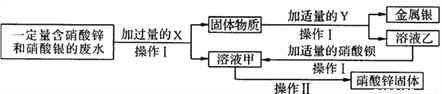
①固体物质的成分有哪些____________?
②写出乙与硝酸钡反应的化学方程式_________________?
③操作I和操作Ⅱ中都要用到一种玻璃仪器。该仪器在操作Ⅱ中的作用是什么______________?
Ag和Zn ZnSO4+Ba(NO3)2==BaSO4↓ +Zn(NO3)2 搅拌,防止液体局部温度过高,造成液滴飞溅。 【解析】由流程图分析,要得到金属银和硝酸锌固体,加入的X是过量的锌,过滤后,固体物质是锌和银的混合物,加入稀硫酸将其分离,溶液乙就是硫酸锌溶液;硫酸锌与硝酸钡反应生成硫酸钡白色沉淀和硝酸锌;操作Ⅱ是从溶液中获取晶体,是蒸发结晶,玻璃棒在此过程中的作用是搅拌散热;因此:①固...查看答案和解析>>
科目:初中化学 来源:山东省泰安市2018年中考化学试卷 题型:综合题
以下是初中化学一些基本实验,请根据实验内容回答下列问题:
(1)利用下图进行粗盐中难溶性杂质去除和配制一定质量分数氯化纳溶液的实验。
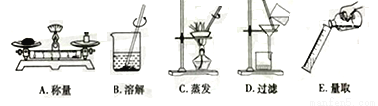
①粗盐中难溶性杂质去除的主要操作顺序是_____________(填字母序号);
②配制11%的氯化钠溶液100g。如按下图进行称量和量取,其它操作均规范无误,最终导致配制的氯化钠溶液的溶质质量分数______(填“大于”、“小于”或”不能确定”)11%。

(2)下图为某小组探究金属化学性质的两组实验。

①实验I中以“金属表面产生气泡的快慢”为标准来判断锌、铁的活动性强弱,有同学认为不够合理,理由是____________________________________;
②写出实验II中C试管内反应的化学方程式____________________________;
③实验II中要验证Cu、Fe、Ag的金属活动性顺序,至少要做的实验是_____ (填字母序号)。
BDC 小于 酸的种类不同 Cu+2AgNO3==2Ag+Cu(NO3)2 CD 【解析】本题考查了粗盐的提纯,配制一定溶质质量分数的溶液,金属的化学性质,化学方程式的书写等。 (1)①粗盐中难溶性杂质去除的主要操作顺序为溶解、过滤、蒸发。故填:BDC; ②如图量取蒸馏水时,仰视读数,会导致量取的水的体积偏大,导致配制的溶液中溶质质量分数小于11% (2)①A中加入的是...查看答案和解析>>
科目:初中化学 来源:山东省泰安市2018年中考化学试卷 题型:单选题
硅是信息技术的关键材料。从石英砂制取芯片的重要反应是SiO2+2C Si +2CO↑,该反应属于
Si +2CO↑,该反应属于
A. 化合反应 B. 分解反应 C. 置换反应 D. 复分解反应
C 【解析】根据化学方程式可知,该反应是由单质与化合物反应生成另一种单质和另一种化合物的化学反应,属于置换反应。故选C。查看答案和解析>>
科目:初中化学 来源:湖北省巴东县2018届九年级第二次质量检测化学试卷 题型:综合题
化学实验和科学探究都离不开实验装置。根据下列装置回答问题:

(1)以上A和B装置都可以用于制取氧气,写出用B装置制取氧气的化学方程式_______;
(2)可用于收集氢气的装置是______(填写序号字母)。
(3)科学探究
(查阅资料)小玲同学查阅资料发现:过氧化钙(CaO2)能分别与水、二氧化碳反应。
(猜想)①过氧化钙与水反应生成氢氧化钙和氧气。
②过氧化钙在空气中久置生成的物质可能是碳酸钙或氢氧化钙或二者的混合物。
(实验探究)
实验一:选用上述实验装置B进行过氧化钙与水反应的实验,收集一试管气体,将带火星的木条伸入试管中,木条复燃;取反应后的溶液置于试管中,充分振荡后再滴入_______(填写一种指试剂的名称)试液,发现溶液变成红色,说明猜想①正确,反应的化学方程式是______。
实验二:为探究猜想②是否正确,小玲设计了如下实验,请你帮助她完成表格中的空白内容:
实验步骤 | 实现现象 | 结论 |
a.取在空气中久置的少量固体于试管中,加足量水 | 未见固体明显溶解 | |
b.向试管中滴加几滴紫色石蕊试液 | 未见明显颜色变化 | 不存在氢氧化钙 |
C. ______ | ______ | 固体成分是碳酸钙 |
实验步骤C中发生反应的化学方程式是______。
D和E 酚酞 另取少量固体于试管中滴加稀盐酸 产生气泡,固体逐渐溶解 【解析】(1)A装置适用于固体和固体加热条件下制取气体,B装置适用于固体和液体常温下制取气体,过氧化氢法制氧气用B装置,反应的化学方程式2H2O22H2O+O2↑;(2)氢气难溶于水,可用排水法收集,使用装置E;氢气的密度比空气的小,可以用向下排空气法收集,可用装置D;【实验探究】实验一:选用过氧化钙与水反应,收集一试管气...查看答案和解析>>
科目:初中化学 来源:湖北省巴东县2018届九年级第二次质量检测化学试卷 题型:单选题
下列有关说法正确的是
A. 我国稀土储量世界第一,可大量开采出口
B. 空气中PM2.5和PM10含量越高说明空气质量越差
C. 酸、碱、盐中可能都不含有氧元素
D. 酸雨是pH<7的降雨
B 【解析】A. 中国稀土资源探明储量占全球的36.52%,是全球第一大稀土资源大国。中国长期大量出口稀土,现在中国用36.4%的储量承担着全球90%以上的稀土供应,为世界稀土市场的供应和稳定作出了巨大贡献。但是近年来由于过度开采和无序竞争,不仅使我国稀土等矿产资源储备大幅下滑,而且给主产地的生态环境造成了巨大破坏,故不应大量开采,错误;B. PM2.5和PM10属于空气污染物。空气中PM2...查看答案和解析>>
科目:初中化学 来源:湖北省利川市2018届九年级第一次质量检测化学试卷 题型:科学探究题
实验室中有一包白色粉末,可能是碳酸钠,也可能是氧化钙或氢氧化钙。为确定其组成,某同学设计了以下实验方案进行探究,请你按要求帮助完成探究活动。
(1)提出假设:
假设① 白色粉末是碳酸钠
假设② 白色粉末是氧化钙
假设③ 白色粉末是氢氧化钙
(2)设计实验,通过实验分析进行判断并填空:
假设 | 设计的相关实验操作 | 实验中观察到的现象 | 假设是否成立 |
① | 取一定量粉末加入稀盐酸 | ____________ | 假设①不成立 |
② | 取一定量粉末溶于水 | 溶液浑浊且温度升高 | 假设②成立 |
③ | 取一定量粉末溶于水,静置后取上层清液再通入二氧化碳 | 没有沉淀产生 | 假设③______ |
(3)实验后思考:假定这包白色粉末是混有少量氧化钙的碳酸钠粉末,将混合物溶于水可观察到的现象是____________;若恰好完全反应,将反应后的混合物进行分离,分离的方法是________;再将分离后的溶液蒸干,得到的固体物质是______(填化学式)。
无气泡产生 , 不成立 , 产生白色沉淀 , 过滤 , NaOH (填化学式) 【解析】(2)①取一定量的粉末加盐酸无气泡产生,说明粉末中没有碳酸钠,故假设①不成立;②取一定量粉末溶于水,溶液浑浊且温度升高,说明粉末中含氧化钙,故假设②成立, ③取一定量粉末溶于水,静置后取上层清液再通入二氧化碳,没有沉淀产生,说明粉末中不含氢氧化钙,故假设③不成立;(3)氧化钙可与水反应生成氢氧化钙,生成...查看答案和解析>>
科目:初中化学 来源:黑龙江省哈尔滨市道里区2018届九年级下学期综合调研测试化学试卷 题型:实验题
请按要求回答下列实验室制取气体并验证气体某些性质的相关问题:
(1)如用高锰酸钾制氧气,反应的化学方程式为_____________________________________;若用排水法收集氧气,如何快速准确判断氧气已经集满_________________________ ;
(2)实验室制取二氧化碳,所用的药品是_______ 和________ ;上述两种药品发生反应使瓶内的气体______,气压变大,__________ ,在压强差的作用下气体从管口逸出;
(3)下图是某同学绘制的制取并验证二氧化碳气体的某些性质的装置图,请补充完整。__________

(4)上图实验成功完成时,B装置中能观察到的现象为__________,能验证二氧化碳气体的性质有_________________。
2KMnO4△ K2MnO4+MnO2+O2↑ 在集气瓶口处冒出1个大气泡 稀盐酸 大理石或石灰石 增多 大于外界压强或大气压 补固体、液体、气泡、露出胶塞少许的导管、橡胶导管 气球上浮、干燥的石蕊纸花不变色,湿润的石蕊纸花由紫色变红色 密度比空气大、能与水反应生成碳酸 【解析】(1)加热高锰酸钾生成锰酸钾、二氧化锰和氧气,反应的化学方程式为:2KMnO4 K2MnO4+MnO2+O2↑;若...查看答案和解析>>
科目:初中化学 来源:北京市平谷区2018届九年级二模化学试卷 题型:流程题
某化工厂的生产流程如下图所示:

(1)生产流程①的基本反应类型是__________反应。
(2)二氧化碳中碳元素的化合价是________。
(3)生产流程④中有关反应的化学方程式为________。
(4)生产流程③中要得到7.4千克熟石灰,至少需加入________千克的水。
分解 +4 Ca(OH)2+Na2CO3 === CaCO3↓+2NaOH 1.8 【解析】 本题通过碳酸钙、生石灰、熟石灰之间的转化,考查了反应类型的判定,有关化合价的计算,根据化学方程式的计算,化学方程式的书写。 (1)生产流程①是碳酸钙高温下分解生成氧化钙和二氧化碳,该反应是由一种物质生成物两种物质,基本反应类型是分解反应; (2)二氧化碳中氧元素的化合价是-2,设:...查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com