
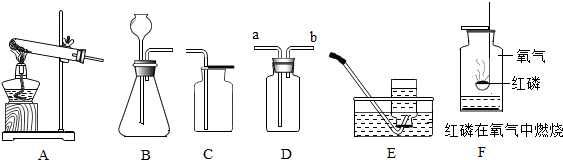
分析 制取装置包括加热和不需加热两种,如果用双氧水和二氧化锰制氧气就不需要加热,如果用高锰酸钾或氯酸钾制氧气就需要加热.氧气的密度比空气的密度大,不易溶于水,因此能用向上排空气法和排水法收集.若用装置D收集氧气,验满方法是:将带火星的木条平放在b管口处,木条复燃,证明氧气满了;实验室制取CO2,是在常温下,用大理石或石灰石和稀盐酸制取的,碳酸钙和盐酸互相交换成分生成氯化钙和水和二氧化碳,因此不需要加热.二氧化碳能溶于水,密度比空气的密度大,因此只能用向上排空气法收集.欲使用装置D用排空气法收集二氧化碳,则气体应从长管进入,因为二氧化碳的密度比空气大;欲使用装置D用排水法收集氧气,并测定收集到的氧气的体积,应先将瓶中装满水,再将气体从短管进入,因为氧气的密度比水小;还需要用到的仪器是量筒;已知一氧化氮气体难溶于水,在空气中容易与氧气发生反应,因此一氧化氮只能用排水法收集;红磷在氧气中剧烈燃烧,冒出大量的白烟,放出热,而瓶底预先放入少量水的目的是:防止污染空气.
解答 解:(1)如果用双氧水和二氧化锰制氧气就不需要加热,过氧化氢在二氧化锰做催化剂的条件下生成水和氧气,要注意配平;故答案为:B;2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑;将带火星的木条平放在b管口处,木条复燃,证明氧气满了;
(2)欲使用装置D用排空气法收集二氧化碳,则气体应从长管进入,因为二氧化碳的密度比空气大;欲使用装置D用排水法收集氧气,并测定收集到的氧气的体积,应先将瓶中装满水,再将气体从短管进入,因为氧气的密度比水小;还需要用到的仪器是量筒;故答案为:a;b;量筒;
(3)已知一氧化氮气体难溶于水,在空气中容易与氧气发生反应,因此一氧化氮只能用排水法收集;故答案为:E;
(4)红磷在氧气中剧烈燃烧,冒出大量的白烟,放出热,而瓶底预先放入少量水的目的是:防止污染空气;故答案为:冒出大量的白烟;防止污染空气;
点评 本考点主要考查了气体的制取装置和收集装置的选择,同时也考查了化学方程式的书写、气体的验满和性质等,综合性比较强.气体的制取装置的选择与反应物的状态和反应的条件有关;气体的收集装置的选择与气体的密度和溶解性有关.本考点是中考的重要考点之一,主要出现在实验题中.


 名校课堂系列答案
名校课堂系列答案科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题

| (I) | (II) | (III) | (IV) | |
| 现象 | 紫色纸花变红 | 紫色纸花不变色 | 紫色纸花不变色 | 紫色纸花变红 |
分析 | ①验(III)验证了:二氧化碳不能使紫色石蕊变红 实验(Ⅳ)验证了;二氧化碳的水溶液能使紫色石蕊变红 ②通过实验(I)、(Ⅳ),可验证酸的一条化学性质是:酸能使紫色石蕊溶液变红 ③实验(Ⅳ)结束后,将纸花用酒精灯小心加热烘烤后纸花又变紫,说明碳酸热稳定性差,受热易分解. | |||
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 在试管中加热KMnO4时,试管口略向下倾斜 | |
| B. | 做铁丝在氧气中燃烧的实验时,集气瓶中预先放少量水 | |
| C. | 用排空气法收集二氧化碳时,导管伸入集气瓶至接近底部 | |
| D. | 用KClO2制O2,排水法收集时,实验完毕后先将导管移出水槽再停止加热 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题

| 实验 装置 | |
| 实验 现象 | ①无水硫酸铜粉末逐渐由白色变为蓝色 ②澄清石灰水变浑浊 |
| 结论 | 久置的镁粉中除镁元素外,还含有的元素是C、H、O 久置的镁粉中含有碱式碳酸镁 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com