
分析 根据化学方程式计算和铁的质量计算出硫酸的质量和氢气的质量,进而求稀硫酸溶液中溶质的质量分数.
解答 解:设稀硫酸溶液中溶质的质量为x,生成氢气的质量为y
Fe+H2SO4=FeSO4+H2↑
56 98 2
5.6g x y
$\frac{56}{5.6g}=\frac{98}{y}=\frac{2}{y}$
x=9.8g,y=0.2g
稀硫酸溶液中溶质的质量分数:$\frac{9.8g}{50g}×100%$=19.6%
答:(1)稀硫酸溶液中溶质的质量分数为19.6%;
(2)反应后所产生氢气的质量为0.2g.
点评 本题主要考查学生对溶质质量分数的计算能力.学生需正确书写出化学方程式,并能正确运用溶质质量分数公式进行计算,才能正确答题.


 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源: 题型:选择题
| A. | C4H12S2 | B. | C2H6 | C. | C2H6O2 | D. | C2H6S |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
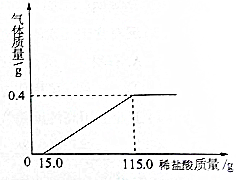 现有12.8g已生锈的铁片,将其放入一定浓度的稀盐酸中充分反应,测得产生的气体质量与稀盐酸的质量关系如图所示(假设铁片除有铁锈外,不含其他杂质),回答:
现有12.8g已生锈的铁片,将其放入一定浓度的稀盐酸中充分反应,测得产生的气体质量与稀盐酸的质量关系如图所示(假设铁片除有铁锈外,不含其他杂质),回答:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com