

| A. | t1℃时烧杯中甲、乙两物质形成的溶液是不饱和溶液 | |
| B. | t2℃时乙物质的溶解度是130g | |
| C. | t2℃时烧杯中甲物质溶液的质量是110g | |
| D. | t1℃时烧杯中甲、乙两物质形成的溶液溶质质量分数约为16.7% |
分析 根据固体物质的溶解度曲线可以:①查出某物质在一定温度时的溶解度,从而可以确定出形成的溶液是否饱和,②比较不同物质在同一温度时的溶解度大小,从而可以比较出其饱和溶液中溶质的质量分数的大小,③判断物质的溶解度随温度变化的变化情况,从而可以判断温度变化时溶液中量的变化进行分析.
解答 解:A、由于在t1℃时,两种物质的溶解度都是20g,即100g水中最多溶解20g,因此将20g甲和乙分别加入到100g,甲和乙会全部溶解形成饱和溶液,故A错误;
B、根据乙的溶解度曲线不难看出,在t2℃时,乙的溶解度是30g,故B错误.
C、由于甲的溶解度随温度的升高而减小,因此升温至t2℃时,甲的溶解度是15g,甲的饱和溶液中就会析出5g晶体,溶液的质量也就由120g变成115g,故C错误;
D、由于甲和乙都全部溶解,因此形成的溶液中溶质的质量分数为:$\frac{20g}{100g+20g}$×100%=16.7%,故D正确.
故选:D.
点评 本题难度不是很大,主要考查了固体溶解度曲线的意义及根据固体的溶解度曲线解决相关的问题.


科目:初中化学 来源: 题型:选择题
| A. | 75% | B. | 80% | C. | 85% | D. | 90% |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
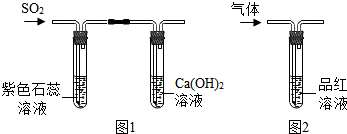
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A.化学与生活 | B.化学与环境 |
| ①生活中常用过滤的方法软化硬水 ②用加热的方法区分热塑性塑料盒热固性塑料 | ①含磷洗涤剂的使用会导致水污染 ②二氧化硫是造成酸雨的原因之一 |
| C.化学与安全 | D.化学与健康 |
| ①在室内放一盆水,可防止煤气中毒 ②夜间发现液化气泄漏开灯寻找泄漏源 | ①食用蔬菜和水果可补充维生素 ②用甲醛的水溶液浸泡海产品保鲜 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | SO${\;}_{4}^{2-}$、NO${\;}_{3}^{-}$、K+、H+ | B. | Na+、Cl-、NO${\;}_{3}^{-}$、Cu2+ | ||
| C. | Na+、K+、NO${\;}_{3}^{-}$、Cl- | D. | Mg2+、Cl-、SO${\;}_{4}^{2-}$、K+ |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | Mg(OH)2不是可燃物 | |
| B. | Mg(OH)2分解吸热,能降低可燃物的温度 | |
| C. | Mg(OH)2分解吸热,能降低可燃物的着火点 | |
| D. | Mg(OH)2分解的产物能使可燃物与氧气隔绝 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
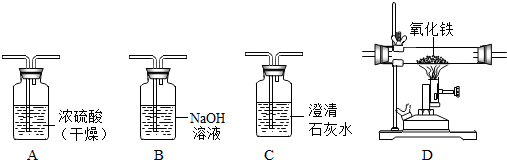
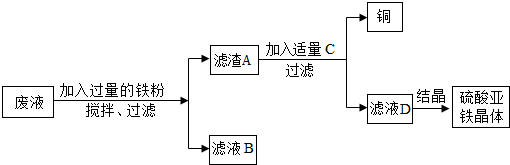
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com