
【题目】如图是甲、乙两种固体物质的溶解度曲线.

(1)由图可获得的一条信息是 .
(2)若乙中混有少量甲,提纯乙的方法是 .
(3)t2℃时,将不饱和的甲溶液,转化成该温度下的饱和溶液的一种方法是 .变化过程中,溶质的质量分数 (选填“增大”、“减小”或“不变”).
(4)将等质量的甲、乙两种物质的溶液由t2℃降温至t1℃时,析出晶体的质量 (选序号).
A.甲>乙 B.甲<乙 C.无法确定.
【答案】
(1)t1℃时,甲和乙的溶解度相等
(2)蒸发结晶
(3)加入溶质或蒸发水分 增大
(4)C
【解析】
试题分析:(1)根据溶解度曲线,获得的一条信息是:t1℃时,甲和乙的溶解度相等或物质甲、乙的溶解度随温度的升高而增大等
(2)根据溶解度曲线,物质乙的溶解度随温度的升高变化不大,故若乙中混有少量甲,提纯乙的方法是蒸发结晶
(3)t2℃时,将不饱和的甲溶液,转化成该温度下的饱和溶液的一种方法是加入溶质或蒸发水分;根据溶质质量分数计算的表达式,变化过程中,溶质的质量分数增大
(4)根据溶解度曲线,物质甲的溶解度随温度的升高变化趋势比物质乙的溶解度随温度的升高变化的趋势要跟大,故将等质量的甲、乙两种物质的饱和溶液由t2℃降温至t1℃时,析出晶体的质量甲>乙,但由于原题并没有注明是饱和溶液,故无法确定,选C


 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源: 题型:
【题目】对下列事实或现象的解释错误的是
选项 | 事实或现象 | 解释 |
A | 八月桂花,十里飘香 | 分子总是在不断运动着 |
B | 水银温度计里的水银热胀冷缩 | 原子大小随温度改变而改变 |
C | 25m3石油气可加压装入0.024m3的钢瓶中 | 分子间是有间隔的 |
D | 一滴水中含千千万万个水分子 | 分子很小 |
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】实验室制取氧气所需装置如图所示,回答下列问题:
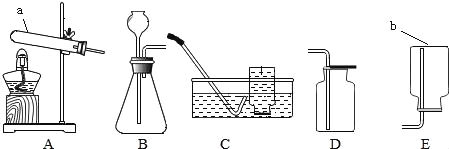
(1)写出仪器名称:b______
(2)用过氧化氢溶液和二氧化锰制取氧气时,其反应的化学方程式______,选用的发生装置是______(填序号),实验结束后装置内得到的物质属于______(填“纯净物”或“混合物”).
(3)碱式碳酸铜是一种绿色粉末,受热条件下发生的反应:Cu2(OH)2CO3![]() 2CuO+H2O+CO2↑,若将干燥的碱式碳酸铜放入______(填序号)装置进行反应,可观察到试管内的实验现象有______、试管口处有小水珠.
2CuO+H2O+CO2↑,若将干燥的碱式碳酸铜放入______(填序号)装置进行反应,可观察到试管内的实验现象有______、试管口处有小水珠.
(4)某兴趣小组查阅资料知:氧化铁也可以作双氧水制取氧气的催化剂,那么氧化铁和二氧化锰这两种物质哪一种更适合呢?他们在探究二氧化锰、氧化铁对过氧化氢分解速率的影响时,他们在控制变量的问题上提出了不同的观点,你认为其中正确的是______(多选).
A.双氧水的浓度一定相同 B.催化剂的质量一定相同
C.反应前双氧水的温度一定相同 D.反应容器的容积一定相同.
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列物质间的转化,能一步实现的是
A. Fe →FeCl3 B. CaCO3 →Ca(OH)2 C. H2O2→ H2 D. Cu(OH)2→CuCl2
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某化学课堂围绕“酸碱中和反应”,将学生分成若干小组,在老师引导下开展探究活动。
【实验】将一定量稀H2SO4加入到盛有NaOH溶液的烧杯中。
【提出问题】实验中未观察到明显现象,部分同学产生了疑问:除水外,反应后溶液中含有哪些物质?
【假设猜想】针对疑问大家提出猜想.甲组同学的猜想如下:
猜想一:只有Na2SO4 猜想二:有Na2SO4 和H2SO4
猜想三:有Na2SO4和NaOH 猜想四:有Na2SO4、H2SO4和NaOH
乙组同学对以上猜想提出质疑,认为有一种猜想是不合理的。不合理的是猜想______。
【实验探究】(1)丙组同学取烧杯中的溶液少量于试管中,滴加几滴酚酞溶液,无明显变化,溶液中一定没有______。
(2)为了验证其余猜想,各学习小组利用烧杯中的溶液,并选用老师提供的pH试纸、铜片、氯化钡溶液、碳酸钠溶液,进行如下三个方案的探究。
实验方案 | 方案一:测溶液pH | 方案二:滴加碳酸钠溶液 | 方案三:向溶液中加入铜片 |
实验操作 |
|
|
|
实验现象 | 试纸变色,对比比色卡,pH<7 | 有气泡产生 | 无气泡冒出 |
实验结论 | 溶液中有H2SO4 | 溶液中有H2SO4 | 溶液中只有Na2SO4 |
【实验结论】写出方案二中反应的化学方程式_________________________。
通过探究,全班同学一致确定猜想 ______是正确的。
【评价反思】老师对同学们能用多种方法进行探究,并且得出正确结论给予肯定。同时指出上面表格中存在两处明显错误,请大家反思。同学们经过反思发现了这两处错误:
(1)实验操作中的错误是_______________________。(说出其中一个即可)
(2)实验中若用氯化钡溶液来进行现象分析,能否得出确切的结论?___为什么?___
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】甲、乙两种物质的溶解度曲线如图所示。下列叙述正确的是
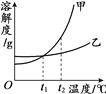
A. 依据溶解度曲线可判断,甲的溶解度比乙的大
B. 将甲、乙的饱和溶液从t2℃降到t1℃,析出甲的质量大
C. t1℃时,甲和乙的饱和溶液各100g,其溶质的质量一定相等
D. 将t2℃时甲的饱和溶液变为不饱和溶液,可采取降温的方法
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】阅读下面科普短文。
锂电池是指电极材料含金属锂或含锂化合物,使用非水溶液做离子导体的电池。银白色的金属锂是所有金属中最轻的一种,它的化学性质活泼,常温下就能和空气中的氧气化合成氧化锂;锂还能和水剧烈反应变成氢氧化锂(LiOH),同时放出一种可燃性气体。
最早出现的锂电池利用化学反应Li+MnO2 LiMnO2提供电能。随着科技的发展,锂电池的应用范围逐步扩大,一类新型锂电池——锂离子电池大量应用在手机、笔记本电脑和家用小电器上。锂离子电池由正极、负极、隔膜和电解液构成,正极材料(如石墨)和负极材料(如LiCoO2)均能传导电子,电解液在正、负两极之间起输运离子、传导电流的作用。锂离子电池采用一种类似摇椅式的工作原理,充放电过程中锂离子在正负极间来回穿梭,从一边“摇”到另一边,往复循环,实现电池的充放电过程。
由于锂离子电池中包含的电解液多含有机物,普遍存在易燃问题,在过充、过放、短路及热冲击等滥用的状态下,电池温度迅速升高,常常会导致电池起火,甚至爆炸。因此,目前大多数数码产品都会配备相应的保护元件,当检测到电池到达满电状态,会自动切断充电电路。
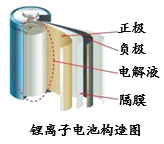
依据文章内容,回答下列问题:
(1)金属锂的物质性质有________________(答一条即可)。
(2)锂离子电池由_______________________________构成。
(3)锂离子电池负极材料为LiCoO2,其中Li为+1价,则Co的化合价为_________。
(4)锂电池使用非水溶液做离子导体的原因是________________________(用化学方程式表示)。
(5)安全使用锂离子电池的措施有______________________________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】当打开一个装有液态空气的容器盖,并将一根燃着的木条置于容器口上方,观察到的现象是
A.燃烧得更旺
B.燃着的木条熄灭
C.先燃烧得更旺后熄灭
D.无明显变化
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com