
| A. | 氧化镁 | B. | 硝酸 | C. | 纯碱 | D. | 苛性钠 |
科目:初中化学 来源: 题型:解答题
 某化学兴趣小组为验证质量守恒定律,取 6.5g锌粒放入烧杯中,向试管内加入 50g稀硫酸,调节天平至平衡(如图所示),然后将稀硫酸全部倒入烧杯中(试管放回),恰好完全反应.试根据要求回答下列问题:
某化学兴趣小组为验证质量守恒定律,取 6.5g锌粒放入烧杯中,向试管内加入 50g稀硫酸,调节天平至平衡(如图所示),然后将稀硫酸全部倒入烧杯中(试管放回),恰好完全反应.试根据要求回答下列问题:查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 石油是一种化工产品 | |
| B. | 将石油分馏可得到多种产品 | |
| C. | 将煤隔绝空气加热可制得焦炭 | |
| D. | 石油可转化成塑料、合成橡胶、合成纤维等 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
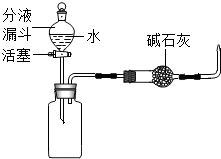 水田或池塘里常常不时地冒出一些气泡,几位同学决心弄清这种气泡的成分.请你与他们一起完成如下的探究:
水田或池塘里常常不时地冒出一些气泡,几位同学决心弄清这种气泡的成分.请你与他们一起完成如下的探究:查看答案和解析>>
科目:初中化学 来源: 题型:填空题
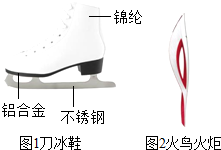 在2014年索契冬季奥运会上,中国运动员共获得了九枚奖牌,成为亚洲体坛霸主.
在2014年索契冬季奥运会上,中国运动员共获得了九枚奖牌,成为亚洲体坛霸主.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com