
| 实验操作方法 | 现象 | 结论 |
| 取少量Na2O2样品置于试管中,加入稀盐酸. | 若产生气体,将产生的气体通入到澄清石灰水,若溶液 变浑浊. | 则说明Na2O2已经变质. |
分析 (1)长期暴露在空气中时,过氧化钠和水反应生成的氢氧化钠会和空气中的二氧化碳反应生成碳酸钠,而过氧化钠和二氧化碳也能直接生成碳酸钠,所以长期暴露在空气中变质生成碳酸钠.确定过氧化钠已经变质就是确定已经生成碳酸钠,所以应该是加入稀盐酸转化得到气体,进而将气体通入澄清石灰水,由于结论是已经变质,则石灰水变浑浊.
(2)生成气体是氧气,可以计算过氧化钠的质量,生成固体是碳酸钙,进而可求算碳酸钠的质量,由于“样品中不考虑水的存在”,所以可求氢氧化钠的质量.
解答 解:
(1)长期暴露在空气中时,过氧化钠和水反应生成的氢氧化钠会和空气中的二氧化碳反应生成碳酸钠,而过氧化钠和二氧化碳也能直接生成碳酸钠,所以长期暴露在空气中变质生成碳酸钠.
由于实验所取样品是实验室放置较长时间的Na2O2样品,所以应该是生成了碳酸钠.确定其变质且得到的结论是已经变质,所以应该是检验碳酸钠的存在,加入的试剂是稀盐酸,生成的气体通入到澄清石灰水中,由于结论是过氧化钠已经变质,所以对应的现象是溶液变浑浊.
(2)生成气体是氧气,可以计算过氧化钠的质量,生成固体是碳酸钙,进而可求算碳酸钠的质量.
设生成1.28g氧气对应的过氧化钠的质量为x
2Na2O2+2H2O═4NaOH+O2↑
156 32
x 1.28g
$\frac{156}{32}$=$\frac{x}{1.28g}$
x=6.24g
生成4.00g碳酸钙需要的碳酸钠的质量为y
Na2CO3+Ca(OH)2=CaCO3↓+2NaOH
106 100
y 4.00g
$\frac{106}{100}$=$\frac{y}{4.00g}$
y=4.24g
由于样品中不考虑水的存在,则12.08g样品中氢氧化钠的质量为12.08g-6.24g-4.24g=1.60g
12.08g上述样品中Na2O2的纯度为$\frac{6.24g}{12.08g}$×100%≈51.7%
故填:(1)Na2CO3; 稀盐酸;澄清石灰水;变浑浊.
(2)51.7%;1.6.
点评 根据化学方程式计算时,第一要正确书写化学方程式,第二要使用正确的数据,第三计算过程要完整.


科目:初中化学 来源: 题型:解答题
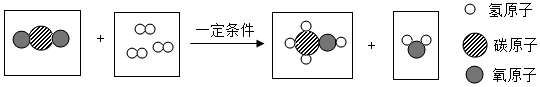
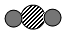 表示的微粒是二氧化碳分子(填名称).
表示的微粒是二氧化碳分子(填名称).查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. |  NaOH固体的保存 | B. | 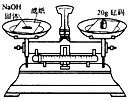 称取NaOH固体 称取NaOH固体 | C. | 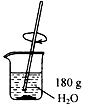 加水溶解 | D. |  装瓶存放 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
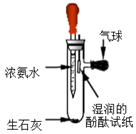 小然同学设计探究分子运动的实验如图,请按要求完成下列各小题:
小然同学设计探究分子运动的实验如图,请按要求完成下列各小题:查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com