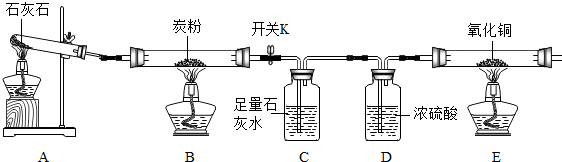
17.如图是某研究性学习小组设计的几种装置,请分析并回答下列问题:
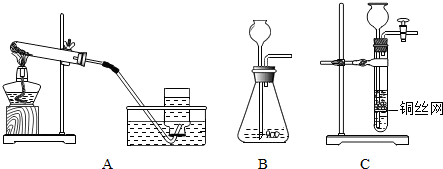
(1)用A装置可制取的气体是氧气,化学反应方程式为2KClO
3$\frac{\underline{MnO_2}}{△}$2KCl+3O
2↑.
(2)B、C两装置都可用作实验室制取O
2、H
2或CO
2的发生装置,写出用此两装置制取其中一种气体的化学方程式CaCO
3+2HCl=CaCl
2+H
2O+CO
2↑.
(3)C装置是在B装置基础上增加隔离铜丝网改进而来的,它的优点是可以控制反应的发生和停止.在实验室制取CO
2时,若隔离网改用铝丝做成,那么产生的后果是生成的气体不纯,其原因是:铝能与盐酸反应生成了氢气,说明金属活动性Cu<Al(选填“>“、“<”或“=“)
(4)该研究性学习小组对用H
2O
2分解生成O
2的实验条件进行探究,发现也可用Fe
2O
3代替MnO
2,且用足量等体积H
2O
2溶液制取相同体积O
2所需时间如下表:
时间 浓度
条件 | 30%H2O2溶液 | 15%H2O2溶液 | 5%H2O2溶液 |
| 加入a g MnO2 | 0.2 | 0.8 | 2.0 |
| 加入a g Fe2O3 | 7.0 | 9.0 | 16.0 |
MnO
2、Fe
2O
3在上述反应中的作用是做催化剂.从上表能得出的结论有①催化剂相同时,H
2O
2溶液的浓度越大反应越快.②不同的催化剂,催化的效果不同.
(5)小童同学在使用“除垢净”去除热水瓶中的水垢时,发现有大量的气泡产生.联想水垢的主要成分是碳酸钙,小明猜想“除垢净”的成分中可能有酸.
①为证实自己的猜想,小童从家中又找来两类不同的物质进行实验:
实验一:将废锌皮(或铁钉等)放入“除垢净”中,有大量气泡产生;
实验二:将生锈铁钉放入到“除垢净”中,铁锈消失且溶液颜色逐步变为黄色.
经实验,小童得出“除垢净”的有效成分中一定有酸的结论.
②小童想试制一瓶“除垢净”,你认为盐酸、硫酸这两种酸中的盐酸更合适,理由是硫酸与水垢反应生成微溶的硫酸钙,除垢不彻底,使用盐酸配制“除垢净”更安全.
③结合上面对“除垢净”的了解,在使用“除垢净”时应注意:去除铝壶中的水垢时,应控制“除垢净”的浓度.

 字词句篇与同步作文达标系列答案
字词句篇与同步作文达标系列答案