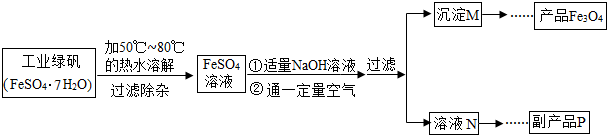
��2011?�����ж�ģ��ij��ȤС���ڸ�ϰ����ұ��ʱ���ڲο������Ϸ�������һ�����֣���֪�ڲ�ͬ���¶��£�CO�����������ﷴӦ��������һ������������������ʣ���CO
2�����Dz������������ʣ��鱾119ҳ��ʵ���У�CO��Fe
2O
3��Ӧ���ɵĺ�ɫ���������Fe�����������ǽ���������̽����
���������ϡ�
����һ��Fe�ۺ�Fe
3O
4��ĩ�ܱ�����������FeO����ɫ�����ܣ�
���϶���Fe
3O
4����Ԫ����+2��+3���ֻ��ϼۣ��仯ѧʽ����FeO?Fe
2O
3 ����ʽ��ʾ��
��������롿��ɫ���ʿ�����Fe
3O
4��FeO��Fe���е�һ�ֻ��֣�
������ʵ�顿��ȤС���ռ���CO��Fe
2O
3��Ӧ���ɵĺ�ɫ���ʽ���������ʵ�飺
|
ʵ�鷽�� |
ʵ������ |
| �� |
ȡ������ɫ�����ô������� |
��ɫ����ȫ������������ |
| �� |
ȡ������ɫ���ʼ���30%�ȵ������� |
�����ݡ���Һ��ɫ��ɻ���ɫ |
| �� |
ȡ������ɫ���ʼ�������ͭ��Һ�� |
������� |
��ʵ����ۡ�
��1����ʵ������˵����ɫ������û��
FeO
FeO
���ҡ���ʵ������˵����ɫ������û��
Fe
Fe
��
��2�����ɵĺ�ɫ����ӦΪFe
3O
4��
��3��д����ɫ��ĩ���ȵ����ᷴӦ�Ļ�ѧ����ʽ
Fe3O4+8HCl�TFeCl2+2FeCl3+4H2O
Fe3O4+8HCl�TFeCl2+2FeCl3+4H2O
��
����չ̽����ͬѧ�Ƕ�Fe
3O
4��������Ȥ���Ӳο��������ҵ�������������������ӡ�øߵ�Fe
3O
4�۵Ĺ������̼�ͼ��
���������̡�
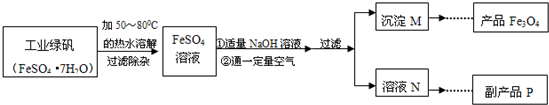
���������ϡ�
����һ�����������ڲ�ͬ�¶��µ��ܽ�����±���ʾ��
| �¶�/�� |
0 |
10 |
30 |
50 |
60 |
70 |
80 |
90 |
| �ܽ��/g |
14.0 |
17.0 |
25.0 |
33.0 |
35.3 |
33.0 |
30.5 |
27.0 |
���϶���Fe��OH��
2������������Ӧԭ��Ϊ��4Fe��OH��
2+2H
2O+O
2=4Fe��OH��
3�����������Fe
3O
4�ķ�Ӧԭ��Ϊ��Fe��OH��
2+2Fe��OH��
3Fe
3O
4+4H
2O
���������ۡ�
��1���ܽ�ʱ����50����80�����ˮĿ����
��50�桫80��ʱ�������������ܽ�Ƚϴ��������ܽ�ĸ��࣬��߲���
��50�桫80��ʱ�������������ܽ�Ƚϴ��������ܽ�ĸ��࣬��߲���
��
��2��д����������NaOH��Һʱ������Ӧ�Ļ�ѧ����ʽ
2NaOH+FeSO4�TFe��OH��2��+Na2SO4
2NaOH+FeSO4�TFe��OH��2��+Na2SO4
��
��3�����������У�Ҫ���ơ�ͨһ������������Ŀ����
����Fe��OH��2ת��ΪFe��OH��3����[���ֹFe��OH��2��ȫת��ΪFe��OH��3]
����Fe��OH��2ת��ΪFe��OH��3����[���ֹFe��OH��2��ȫת��ΪFe��OH��3]
��
��4��Ҫʹ�����������IJ�����ߣ������������в�����Fe��OH��
2��Fe��OH��
3�����������Ϊ
90��214����45��107��
90��214����45��107��
��
��5������ƷP�������ƣ�����ҺN��øø���Ʒ�IJ���˳����b��
c
c
��
a
a
��d��
a������ b������Ũ�� c����ȴ�ᾧ d�������������ȫʧȥ�ᾧˮ
�����ȷ����Ϊȷ�������Ϸ����Ƶõ������������п��ܺ��е����ʣ�ͬѧ���ֽ���������ʵ��̽����
���������ϡ�
����һ�������Լ�����ʱ�ֽܷ���������������ˮ����Ӧ�и���Ԫ�صĻ��ϼ۲��䣩��
���϶���Fe
2O
3��CO��Ӧ�����¶����߶����еģ�������Fe
3O
4��������FeO����ɫ�����������Fe��
��������롿Fe
3O
4�п��ܺ��е�������Fe
2O
3��FeO�е�һ�ֻ����֣�
��ʵ����ơ�ͬѧ�dz�ȡ��23.28g��Fe
3O
4��Ʒ����������ʵ�飺
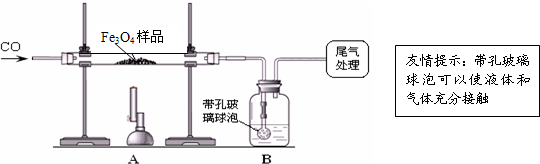
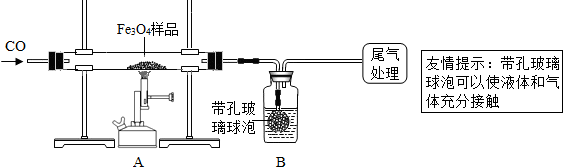
��ʵ���������̽��˼·��ͬ����ȤС��ֳɼס�����С�飮
���飺
��1������ͬѧ��ͨ��Bװ�÷�Ӧǰ��������仯������ȷ�ϸ�Fe
3O
4��Ʒ�е����ʣ�B�е�����Լ���_
��
��
������ţ���
�ٳ���ʯ��ˮ ����������Ũ��Һ ��ϡ���� ��ˮ
��2������ʵ������У�CO�������Ϊ��Ӧ���⣬�����������ǣ���ʵ�鿪ʼʱ���ž�װ���еĿ�������ֹ����ʱ������ը����ֹͣ���Ⱥ�ֹA�������ﱻ������B�е���Һ������A�У���
��װ���е�CO2����NaOH��Һ��
��װ���е�CO2����NaOH��Һ��
��
��3������ͬѧ��ΪBװ�÷�Ӧǰ���
�������ƫС��Ӱ����㡢����������Ϊ���ǵ�������
CO��B����Һ���ݳ�ʱ���������ˮ����
CO��B����Һ���ݳ�ʱ���������ˮ����
��
���飺
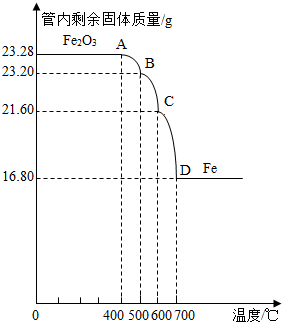
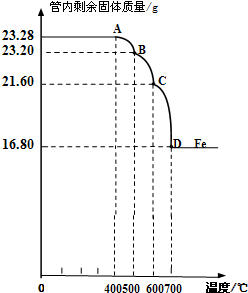
���������ⶨ�����Ƴɷ�Ӧ������Aװ���в������ڵĹ����������¶ȵı仯���ߣ���ͼ����
��1��д��BC�η�����Ӧ�Ļ�ѧ����ʽ��
��
��2��ͨ������ȷ������Fe
3O
4��Ʒ�к��е�������
Fe2O3
Fe2O3
�����к�Fe
3O
4��������
20.88
20.88
g��������Ҫд���̣�



 ��У����ϵ�д�
��У����ϵ�д�


 �������ƫС��Ӱ����㡢����������Ϊ���ǵ�������
�������ƫС��Ӱ����㡢����������Ϊ���ǵ�������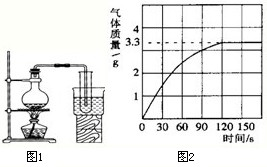 ˮ����Ҫ����Դ�����˼�һ����������������ģ���Ȼ���ˮ���и������ʣ�������ֱ��ʹ�ã�����о�����
ˮ����Ҫ����Դ�����˼�һ����������������ģ���Ȼ���ˮ���и������ʣ�������ֱ��ʹ�ã�����о�����