
【题目】根据如图所示的实验回答问题。
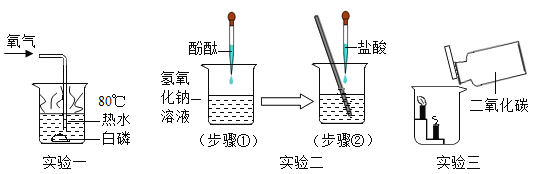
(1)实验一通入氧气后,观察到的现象是_____,说明燃烧需要的条件是_____。
(2)实验二滴加酚酞溶液的目的是_____,反应的化学方程式为_____。
(3)燃烧的蜡烛由低到高依次熄灭,说明二氧化碳的性质有_____。
【答案】热水中的白磷燃烧 燃烧需要氧气 指示酸碱发生了中和反应 NaOH+HCl=NaCl+H2O 密度比空气大,既不能燃烧,也不支持燃烧
【解析】
(1)实验一通入氧气后,观察到的现象是热水中的白磷燃烧,根据通入氧气前后的对比,说明燃烧需要的条件是氧气。故填:热水中的白磷燃烧;燃烧需要氧气。
(2)实验二盐酸与氢氧化钠发生了中和反应,其反应方程式为:NaOH+HCl=NaCl+H2O,在烧杯中滴加酚酞溶液的目的是:指示酸碱发生了中和反应;故填:指示酸碱发生了中和反应;NaOH+HCl=NaCl+H2O。
(3)将二氧化碳慢慢倒入烧杯中,观察到蜡烛由低到高依次熄灭的现象,所以说明二氧化碳具有的性质是密度比空气大(物理性质),不助燃、不可燃(化学性质);故填:密度比空气大,既不能燃烧,也不支持燃烧。


科目:初中化学 来源: 题型:
【题目】用纳米级的某种氧化物做催化剂,可使汽车尾气中的 CO 和 NO 迅速反应转化为两种常见气体,其中一种是空气中含量最多的气体。能正确表示该反应的化学方程式是 。
A.
B.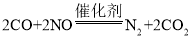
C.![]()
D.
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】目前,我们国家的能源主要依赖于化石燃料,它们属于不可再生资源。因此,开发利用新能源就显得格外重要。
(1)常见的三种化石燃料包括石油、煤和____________。
(2)利用新能源发电的类型有潮汐能发电、地热能发电、_______________等(请举一例)。
(3)在新能源汽车未普及时,如图所示为一种“节能减排”的有效措施。请写出乙醇充分燃烧的化学方程式_________。

(4)在催化剂作用下,乙醇与氧气、氢氧化钠在燃料电池中反应生成水和另一种物质,并得到电能,请你完成该反应的化学方程式: ________
________![]() .
.
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】黄铁矿的主要成分为二硫化亚铁(FeS2),工业上可利用黄铁矿煅烧的产物冶炼铁和生产浓硫酸,其工业流程如图:

下列说法错误的是( )
A. 反应②不是置换反应,反应③④为化合反应
B. 反应①中各元素的化合价均发生了改变
C. 该工业生产过程产生的废气中的SO2可以用熟石灰溶液吸收
D. 向制得的100克98%的浓硫酸中加入100克蒸馏水,配制49%的稀硫酸
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列变化与对应的图像关系正确的是
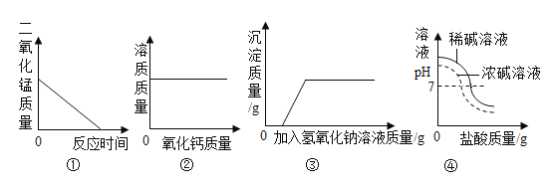
A.图①是给氯酸钾和二氧化锰的混合物加热
B.图②是向一定温度下的饱和氢氧化钙溶液中不断加入氧化钙固体
C.图③是向氯化铜和稀盐酸的混合溶液中加入氢氧化钠
D.图④是将相同质量分数的稀盐酸滴入到等体积不同质量分数的 NaOH 溶液
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某化学兴趣小组同学按如图操作完成粗盐(含有难溶性杂质)提纯实验。下列说法正确的是 ( )
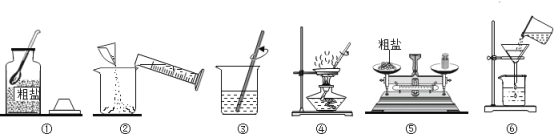
A.所得精盐潮湿会使产率偏低B.④操作中待溶剂全部蒸干后再停止加热
C.去除难溶性杂质的步骤是③D.正确的操作顺序为①⑤②③⑥④
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某兴趣小组对KClO3分解反应的催化剂进行研究,在相同的加热条件下,用下图装置完成表中实验:

编号 | KClO3质量/g | 催化剂 | 催化剂质量/g | 收集50mLO2所需时间/s |
实验1 | 5 | - | - | 171 |
实验2 | 5 | MnO2 | 0.5 | 49 |
实验3 | 5 | Fe2O3 | 0.5 | 58 |
实验4 | 5 | KCl | 0.5 | 154 |
(1)设置实验1的目的是___________________
(2)表中所列3种催化剂的催化效果最佳的是______________
(3)写出KClO3分解的化学方程式:_________________________
(4)由实验1和实验4可知,KCl____(填“有”或“无”)催化作用。维持加热条件不变,用实验1再继续收集收集50mLO2,所需时间明显少于171s,解释原因:_____________
(5)要比较KClO3分解反应中不同催化剂的催化效果,除了测量收集50mLO2所需时间外,还可以测量相同时间内____________
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】为测定某氧化铜和铜的固体混合物中氧化铜的质量分数,小勇同学取20g固体混合物置于烧杯中,将100g稀硫酸分为四等份依次加入其中进行实验,测得数据如下:
次序 | ① | ② | ③ | ④ |
加入稀硫酸的质量/g | 25 | 25 | 25 | 25 |
剩余固体的质量/g | 16 | a | 10 | 10 |
回答列问题:
(1)原固体混合物中,氧化铜的质量分数为_____。
(2)上表中,a的值为_____,实验③所得溶液中的溶质是_____(填化学式)。
(3)该实验所用稀硫酸中溶质的质量分数为____。(写出计算过程,结果精确到0.1%)
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】水与溶液在生产生活中有广泛的用途。
(1)将硬水转化为软水的原理是将硬水中溶有较多含________(填元素符号,下同)、________的物质除去。
(2)在水中加入洗涤剂可增强去油污的能力,这是因为洗涤剂有________作用。
(3)自热米饭是利用发热包中的生石灰与水反应放出热量来进行加热,生石灰与水反应的化学方程式为________ 。
(4)如图为甲、乙、丙三种物质的溶解度曲线。

①在30℃时,向30g甲物质中加入50g水,充分搅拌后,需再加入________g水恰好形成饱和溶液。
②若甲中混有少量乙,采用________的方法提纯甲。
③30℃时,将甲、乙、丙的饱和溶液降温到10℃,所得溶液的溶质质量分数最小的是_______。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com