


分析 (1)根据双氧水的不稳定性分析
(2)根据碳酸钠或双氧水的化学性质分析
(3)①根据化学方程式,已知氧气的质量,可以求出碳酸钠的质量.
②分析反应的过程可知:加入的碳酸钠先与盐酸反应,把盐酸消耗完了,才开始与氯化钙反应,开始生成沉淀,最后到达最高点说明已经反应完了,据此分析解答.
解答 解:(1)双氧水在二氧化锰作用下分解生成水和氧气,化学方程式为:2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑;双氧水在常温下就能分解,所以在反应前加入稳定剂的作用是防止双氧水分解.
(2)导致碳酸钠变质的原因是与碳酸钠或双氧水反应了,A、加入二氧化锰,使双氧水分解而变质;B加入稀盐酸,与碳酸钠反应而变质;C加入硫酸钠,不能与碳酸钠与双氧水反应,不变质;D加入石灰水,与碳酸钠反应生成碳酸钙和氢氧化钠;故选C.
(3)①设生成Na2CO3的质量为x
2(2Na2CO3•3H2O2)═4Na2CO3+6H2O+3O2↑
424 96
x 12g
$\frac{424}{x}=\frac{96}{12g}$
x=53g
②根据题意可知碳酸钠先与盐酸反应,再与氯化钙反应,由图示可知碳酸钠与盐酸反应生成气体2.2g,碳酸钠与氯化钙反应,生成沉淀5.0g.设生成2.2g气体所需的Na2CO3的质量为y,生成沉淀5.0g所需Na2CO3的质量为z.则
Na2CO3~CO2↑
106 44
y 2.2g
$\frac{106}{y}=\frac{44}{2.2g}$,
解得y=5.3g;
Na2CO3~CaCO3↓
106 100
z 5.0g
$\frac{106}{z}=\frac{100}{5.0g}$,
解得z=5.3g;
所以x=(5.3g+5.3g)÷10%=106g,
故答案为(1)2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑;防止双氧水分解.(2)C.
(3)①生成Na2CO3的质量为53g,②106g.
点评 本题考查了双氧水、碳酸钠的化学性质及有关溶液及化学方程式的计算,注重考查学生的分析能力和基本计算能力.


 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源: 题型:实验探究题
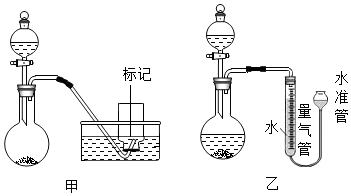
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. |  加热一定量高锰酸钾的实验,试管中固体的质量变化 | |
| B. | 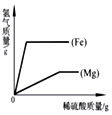 等质量的镁条和铁丝分别与足量的稀硫酸反应,产生气体的质量变化 | |
| C. |  向一定质量的水中加入氢氧化钠时,形成的溶液pH的变化 | |
| D. | 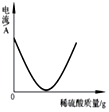 向盛有一定量Ba(OH)2溶液的烧杯中逐滴滴加稀硫酸,测得烧杯中溶液导电性的变化 |
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
 为研究影响化学反应快慢的因素,小明选取成分相同的大理石碎屑、块状大理石两种样品各6克,分别与足量的、溶质质量分数相同的稀盐酸在锥形瓶中反应(样品中杂质不与稀盐酸反应),实验装置如右图所示.每2分钟读取一次电子天平的示数,据此计算生成的二氧化碳的质量,前18分钟数据记录见下表:
为研究影响化学反应快慢的因素,小明选取成分相同的大理石碎屑、块状大理石两种样品各6克,分别与足量的、溶质质量分数相同的稀盐酸在锥形瓶中反应(样品中杂质不与稀盐酸反应),实验装置如右图所示.每2分钟读取一次电子天平的示数,据此计算生成的二氧化碳的质量,前18分钟数据记录见下表:| 时间/分 | 0 | 2 | 4 | 6 | 8 | 10 | 12 | 14 | 16 | 18 |
| 大理石碎屑生成的C02质量/克 | 0 | 1.45 | 1.75 | 1.98 | 2.18 | 2.30 | 2.36 | 2.40 | 2.40 | 2.40 |
| 块状大理石生成的C02质量/克 | O | 0.45 | 0.80 | 1.10 | 1.36 | 1.60 | 1.81 | 1.98 | 2.11 | 2.20 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 化合物 | B. | 混合物 | C. | 非金属单质 | D. | 金属单质 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | AB2 | B. | A2B3 | C. | A2B5 | D. | A2B6 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com