
 CaO+CO2 ↑。若要制取2.8吨生石灰,至少需要含杂质10%(杂质不参加反应)的石灰石多少吨?(结果保留一位小数)
CaO+CO2 ↑。若要制取2.8吨生石灰,至少需要含杂质10%(杂质不参加反应)的石灰石多少吨?(结果保留一位小数)科目:初中化学 来源:不详 题型:计算题
查看答案和解析>>
科目:初中化学 来源:不详 题型:计算题
查看答案和解析>>
科目:初中化学 来源:不详 题型:计算题

| | 反应前 | 反应后 |
| Ⅰ 组 | 玻璃管和红色粉末的总质量为48.3 g | 玻璃管和固体物质的总质量为47.1 g |
| Ⅱ 组 | 洗气瓶和瓶中所盛物质的总质量为258.6 g | 洗气瓶和瓶中所盛物质的总质量为261.9 g |
查看答案和解析>>
科目:初中化学 来源:不详 题型:计算题

查看答案和解析>>
科目:初中化学 来源:不详 题型:计算题
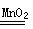 2H2O+O2↑)
2H2O+O2↑)查看答案和解析>>
科目:初中化学 来源:不详 题型:单选题
| A.0.03%<ω<2% | B.0.6%<ω<0.87% |
| C.2.48%<ω<3.6% | D.6.2%<ω<9% |
查看答案和解析>>
科目:初中化学 来源:不详 题型:单选题
| A.4.4克 | B.8.8克 | C.2.2克 | D.4.0克 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com