
【题目】在“宏观一微观”之间建立联系。是学习化学学科必备的思维方式。下图是某反应的微观示意图,下列说法正确的是
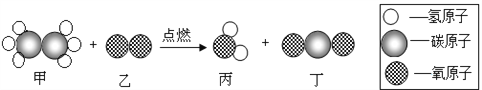
A. 该反应中甲、乙、丙、丁都属于化合物 B. 参加反应的甲、乙的质量比为60:224
C. 反应生成丙、丁分子个数比为1:1 D. 该反应不遵守质量守恒定律
科目:初中化学 来源: 题型:
【题目】根据图中实验装置,回答问题:
发生装置 | 收集装置 | 洗气装置 |
|
|
|
(1)仪器a的名称是________.
(2)用A装置制取氧气的化学方程式为________,收集装置为(填字母序号)________.
(3)实验室制取二氧化碳的化学反应方程式为________,若用F装置收集二氧化碳,则气体应从F装置的________(填“①”或“②”)端口通入.
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某研究小组为探究“影响铁制品锈蚀快慢的因素”,取同浓度的稀氨水和稀醋酸,用右图装置完成表中实验,回答下列问题。
![]()
实验序号 | ① | ② | ③ | ④ |
实验温度/℃ | 25 | 25 | 70 | 70 |
试剂 | 稀氨水 | 稀醋酸 | 稀氨水 | 稀醋酸 |
出现铁锈 所需时间 | 1天 未见锈蚀 | 5分钟 | 1天 未见锈蚀 | 1分钟 |
(1)铁锈的主要成分是________(填化学式)。
(2)实验②和④可探究________因素对铁制品锈蚀快慢的影响;欲探究试剂酸碱性对铁制品锈蚀快慢的影响,应选择的实验是______________(填实验序号)。
(3)根据表中实验现象得出的结论是_________________(写出1点即可)。
(4)影响铁制品的锈蚀快慢除上述因素外,还有______________________(写出1点即可),请设计实验方案_________________________________________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如下图是一个“珠漏“,A首先漏下,A﹣F分别代表6种初中化学的常见物质:氧气、木炭、碳的某种氧化物、铁、氧化铁、硝酸银。
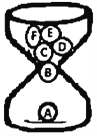
珠子漏下的规律:
①相对分子质量最大的第一个漏下;
②先漏下的珠子带动下一颗相互间能反应的珠子漏下,从而实现按A﹣B﹣C﹣D﹣E﹣F的顺序漏下。
(1)请写出以下物质的化学式A_____E_____。
(2)“碳的某种氧化物”是_____,它是A~F中的_____。
(3)请写出A与B反应的化学方程式_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】兴趣小组的同学想测定某石灰石样品中碳酸钙的质量分数,他们取9克石灰石于烧杯中并慢慢加入盐酸,测得反应过程剩余固体质量与加入盐酸的质量关系如下图所示(石灰石中的杂质不与盐酸反应也不溶于水)
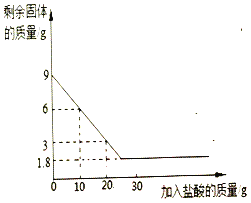
请回答下列问题:
(1)石灰石中所含杂质的质量是_____g
(2)通过计算求所用石灰石中含碳酸钙的质量分数以及生成二氧化碳质量_____、_____(该结果精确到0.1g)
(3)当加入_____克盐酸时,反应恰好停止。
(4)根据以上数据画出产生的气体与加入的盐酸质量的关系图__________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下图中甲、乙、丙、丁、戊表示初中化学几种常见的物质,且分别是由O、C、Fe、Cu中的一种或两种元素组的。在通常情况下,甲、乙、丙与其他物质的状态不同,其中乙、丙为化合物,丙中两种元素质量之比为3:8;戊为紫红色固体,图中“一”表示两端的物质间能够发生化学反应,“→”表示物质间存在转化关系;部分反应物、生成物或反应条件已略去。下列判断中,错误的是
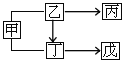
A. 丙的化学式CO2 B. 乙可作为燃料
C. 丁→戊的转化基本反应类型属置换反应 D. 甲的化学式为CO
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】铜在潮湿的空气中会生锈生成铜绿,铜绿的主要成分为碱式碳酸铜(化学式:Cu2(OH)2CO3),
铜绿的成分有多种,其化学式也可表示为xCu(OH)2·yCuCO3。
(1)孔雀石呈绿色,是一种名贵的宝石,其主要成分是Cu(OH)2·CuCO3。某兴趣小组为探究制取孔雀石的最佳反应条件,设计了如下实验:
(已知:2Cu(NO3)2+2NaOH+Na2CO3===Cu(OH)2·CuCO3↓+4NaNO3
实验1:将2.0mL9.0%的Cu(NO3)2溶液、2.0mlL2.0%的NaOH溶液和2.0%的Na2CO3溶液按表I所示体积混合,实验记录如下
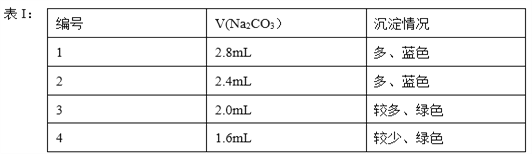
实验2:将合适比例的混合物在表Ⅱ所示温度下反应,实验记录如下。
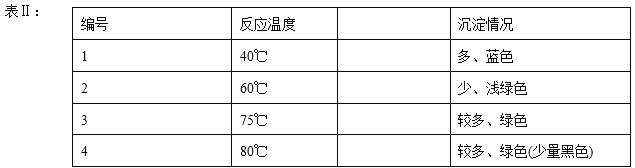
①为了避免铜生锈,铜应尽量保存在______________________;
②实验室制取少许孔雀石,应该采用的最佳温度条件是_______________;
③80℃时,所制得的孔雀石有少量黑色物质的可能原因是_____________。
(2)实验小组为测定上述某条件下所制得孔雀石(xCu(OH)2·yCuCO3)样品组成,利用下图所示的装置(夹持仪器省略)进行实验: (已知:碱石灰能吸收二氧化碳和水,浓硫酸有吸水性)
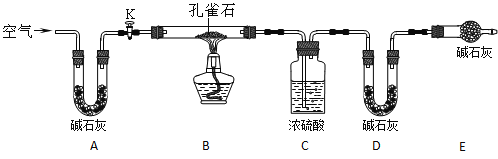
①装置E中碱石灰的作用是____________________;
②充分反应后,某同学在实验过程中采集了如下数据:
a.反应前玻璃管与样品的质量163.8g; b.反应后玻璃管中残留固体质量56.0g;
c.装置C实验后增重9.0g; d.装置D实验后增重8.8g
根据上述有关数据及计算结果,写出该样品组成的化学式______________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】地壳中含有丰富的氧、硅、铝、铁等元素.如图是四种元素的有关信息,关于四种元素的说法错误的是( )

A.氧元素的原子序数为8
B.铁元素属于金属元素
C.铝元素的原子在化学反应中易失去电子
D.硅元素的相对原子质量为28.09g
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】臭氧(O3)是对于环境有重要影响的物质,兴趣小组对其进行如下探究。
【查阅资料】①O3微溶于水:
②O3常用于消毒等,但浓度超标时对人体有毒副作用;
③品红溶液为红色,遇强氧化剂(如O3)会变味无色。
探究一·臭氧的制备
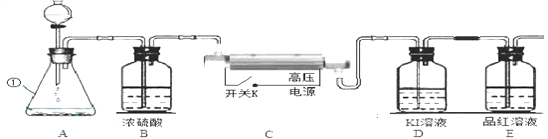
(1)写出仪器①名称___________。
(2)图中A装置制取氧气的化学方程式是______________。
(3)将A中制得的氧气一次通过图中B→E装置。
①B中浓硫酸的作用是____________________。
②实验开始,先通过一段时间氧气,合上C装置电源开关,在电火花作用下O2会转化为O3,该反应是____(填“物理”或“化学”)变化。
探究二·臭氧含量的测定
D中反应原理为:2KI+O3+H2O 2KOH+I2+O2,当E中出现现象时,可知D中反应完全。从安全、环保角度看,上述装置不足之处是____________。
(6)若D中生成碘12.7mg,则理论上应吸收O3_______mg(O3、I2的相对分子质量分别为48.254)。
探究三·影响臭氧分解的因素
O3在水中易分解,一定条件下,某浓度的O3在浓度减少一半所需的时间(t)如下表所示。
温度 分钟 pH | 3.0 | 4.0 | 5.0 | 6.0 |
20 | 301 | 231 | 169 | 58 |
30 | 158 | 108 | 48 | 15 |
40 | 31 | 26 | 15 | 7 |
(7)①分析表中数据,臭氧的分解速率与___________、___________有关。
②据表推测O3在下列条件下分解速率从小到大的顺序为___________(填序号)。
a.20℃、pH=3.0 b.30℃、pH=4.0 c.50℃、pH=6.0
③臭氧在水中分解是臭氧与水反应生成氧气和过氧化氢,反应的化学方程式为__________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com