
分析 (1)根据分子之间有间隙所以10mL酒精与10mL水混合,其体积小于20mL分析.
(2)根据分子不断运动导致白酒瓶敞口放置,酒的香味变淡分析.
(3)根据气体分子间的间隔较大,液体和固体分子之间的间隔较小所以气体容易压缩,而液体和固体难以压缩分析.
解答 解:
解:(1)分子之间有间隙所以10mL酒精与10mL水混合,其体积小于20mL.
(2)分子不断运动导致白酒瓶敞口放置,酒的香味变淡,故答案:分子是不断运动的.
(3)气体分子间的间隔较大,液体和固体分子之间的间隔较小所以气体容易压缩,而液体和固体难以压缩,故答案:气体分子间的间隔较大,液体和固体分子之间的间隔较小.
故答案为:(1)分子间有间隔;(2)分子是不断运动的;(3)气体分子间的间隔较大,液体和固体分子之间的间隔较小.
点评 本题难度不大,掌握分子的基本性质及利用分子的基本性质分析和解决问题的方法是解答此类题的关键.


 举一反三同步巧讲精练系列答案
举一反三同步巧讲精练系列答案 口算与应用题卡系列答案
口算与应用题卡系列答案 名师点睛字词句段篇系列答案
名师点睛字词句段篇系列答案科目:初中化学 来源: 题型:实验探究题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
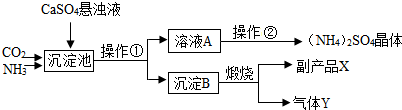
查看答案和解析>>
科目:初中化学 来源: 题型:推断题
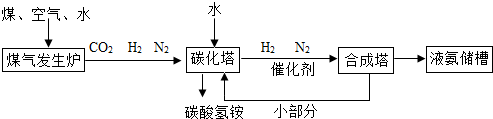
查看答案和解析>>
科目:初中化学 来源: 题型:推断题
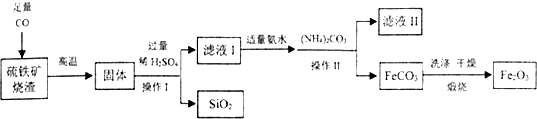
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
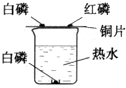 探究燃烧条件的实验装置如图所示.
探究燃烧条件的实验装置如图所示.查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com