
| A、10% | B、8% |
| C、80% | D、20% |
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
| 稀盐酸的用量 | 第一次加入5g | 第二次加入5g | 第三次加入5g | 第四次加入5g |
| 剩余固体的质量 | 3g | 2g | 1g | 1g |
查看答案和解析>>
科目:初中化学 来源: 题型:
| A、炭雕是质轻透明的固体 |
| B、炭雕艺术品可以长久保存 |
| C、炭雕摆放要远离火源 |
| D、炭雕能吸附室内微量的甲醛等有害气体 |
查看答案和解析>>
科目:初中化学 来源: 题型:
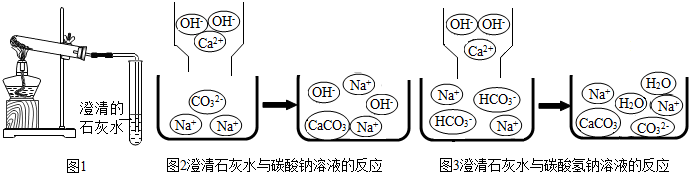
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com