
 金属的使用范围特别广.现探究金属与酸溶液反应快慢与哪些因素有关.陈璐、魏松明、韩俊洋、徐庚辰4位同学分别做了下列实验:
金属的使用范围特别广.现探究金属与酸溶液反应快慢与哪些因素有关.陈璐、魏松明、韩俊洋、徐庚辰4位同学分别做了下列实验:分析 (1)【陈璐实验】根据铝粉比铝片与盐酸接触的充分进行解答;
【魏松明实验】根据镁的金属活动性大于铝进行解答;
【韩俊洋实验】根据反应物的浓度越大,化学反应速率越快进行解答;
【实验结论】根据实验现象进行解答;
(2)①根据活动性强的金属与酸反应放出氢气的速率快进行解答;
②根据金属的相对原子质量与生成的氢气质量成反比进行解答;
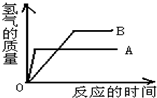
③根据图示可知A的金属活动性大于B,且A的相对原子质量大于B进行解答;
(3)根据铝易被氧气氧化生成氧化铝以及氢气的质量求出铝的质量进行解答;
【反思与评价】根据金属的质量相同,且酸足量的情况下生成的氢气质量相同进行解答.
解答 解:(1)【陈璐实验】铝粉比铝片与盐酸接触的充分,所以用铝片与铝粉分别和稀盐酸反应,发现铝粉反应快,方程式2Al+6HCl=2AlCl3+3H2↑;故填:铝粉;2Al+6HCl=2AlCl3+3H2↑;
【魏松明实验】镁的金属活动性大于铝,所以用镁粉与铝粉分别与稀盐酸反应,发现镁粉反应快;故填:镁粉;
【韩俊洋实验】反应物的浓度越大,化学反应速率越快,所以用镁条分别与10%稀盐酸、15%稀盐酸反应,发现15%稀盐酸反应快;故填:15%稀盐酸;
【实验结论】根据实验现象可知,金属与酸溶液反应快慢与金属的活动性强弱、金属颗粒的大小、酸的浓度等有关;故填:活动性强弱;大小;浓度;
(2)①活动性强的金属与酸反应放出氢气的速率快,由图可知,A金属反应完需要的时间少,所以A、B两种金属的活动性大小是:A>B;故填:A>B;
②金属的相对原子质量与生成的氢气质量成反比,A生成的氢气少,所以A金属的相对原子质量大;故填:A>B;
③根据图示可知A的金属活动性大于B,且A的相对原子质量大于B,所以A、B可能是Zn和Fe;故填:Zn和Fe;
(3)设铝的质量为x
2Al+3H2SO4=Al2(SO4)3+3H2↑
54 6
x 3g
$\frac{54}{x}=\frac{6}{3g}$
x=27g
该铝片中铝元素质量=(32.1g-27g)×$\frac{54}{102}×100%$+27g=29.7g;故填:27;29.7;
【反思与评价】根据金属的质量相同,且酸足量的情况下生成的氢气质量相同,所以等质量的 铝粉 与 铝片 分别与足量的稀硫酸、稀盐酸反应,产生H2 的质量关系是相等.故填:相等;金属的质量相同,且酸足量的情况下生成的氢气质量相同.
点评 掌握金属的活动性强弱顺序以及应用是解题的关键,难度较大.


 口算能手系列答案
口算能手系列答案科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
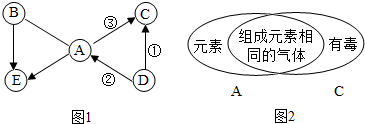 A-E是初中化学常见的物质,E是大理石的主要成分,它们的相互转化关系如图1所示,“-”表示相互间能反应,“→”表示能转化,部分反应条件、反应物、生成物已略去.如图2表示的是A、C的相关信息.请回答下列问题:
A-E是初中化学常见的物质,E是大理石的主要成分,它们的相互转化关系如图1所示,“-”表示相互间能反应,“→”表示能转化,部分反应条件、反应物、生成物已略去.如图2表示的是A、C的相关信息.请回答下列问题:查看答案和解析>>
科目:初中化学 来源: 题型:填空题
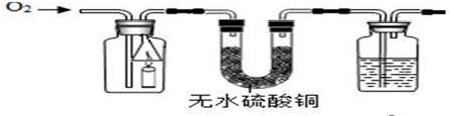
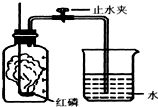 某同学设计了测定空气中氧气含量的实验,实验装置如图.请回答下列问题:
某同学设计了测定空气中氧气含量的实验,实验装置如图.请回答下列问题:查看答案和解析>>
科目:初中化学 来源: 题型:填空题
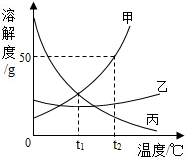 如图是甲、乙、丙三种固体物质的溶解度曲线,请回答:
如图是甲、乙、丙三种固体物质的溶解度曲线,请回答:查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | PM2.5与雾霾天气 | B. | 新装修房屋内空气中的杀手 | ||
| C. | 形成酸雨的罪魁祸首 | D. | 燃气热水器安装在居室内的危险 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com