
����Ŀ����ͼ�Ǽס������ֹ������ʵ��ܽ������ͼ������˵������ȷ����
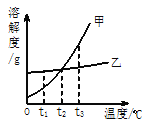
A. t2��ʱ���ס����������ʱ�����Һ��������������һ�����
B. t3��ʱ�����ס��ҵı�����Һ�������� 10g ˮ�������ľ��������������ҵľ���������
C. t1��ʱ���ѼIJ�������Һ��Ϊ������Һ���ܼ�����һ������
D. t3��ʱ�����ס��ҵı�����Һ������ t2�����������������������
���𰸡�AB
��������
A�����ݼס������ֹ������ʵ��ܽ������ͼ��֪��t2��ʱ���ס����������ʵ��ܽ�����߽���һ�㣬�ܽ����ͬ��һ���¶��±�����Һ�����ʷ���=![]() ��������Һ��������������һ����ȣ���A��ȷ��
��������Һ��������������һ����ȣ���A��ȷ��
B�����ܽ�����ߵı仯��֪�����ܽ�����¶ȵı仯���Ҵ�����t3��ʱ�����ס��ҵı�����Һ�������� 10g ˮ�������ľ��������������ҵľ���������B��ȷ��
C��t1��ʱ��ͨ�����£��ɰѼIJ�������Һ��Ϊ������Һ���ܼ��������䣬��C����
D��t3��ʱ�����ס��ҵı�����Һ������ t2�棬������Һ���о����������γ�t2��ʱ�ı�����Һ��t2��ʱ�ס��ҵ��ܽ����ͬ��������������һ����ȣ���D��ȷ����ѡAB��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������Cl2���ھ�ˮ����ҵ��������;�㷺����Cl2�Ʊ�Ư��Һʱ�����·�Ӧ��Cl2+2NaOH�TNaCl+NaClO+H2O����ش��������⣺
��Cl����ԭ�ӽṹʾ��ͼΪ_____��������NaClO����Ԫ�صĻ��ϼ�Ϊ_____��
��20��ʱ��NaCl���ܽ��Ϊ36g�����¶��£�����NaCl��Һ���������ܼ�������֮��Ϊ_____��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������ʵ��װ�ý���ʵ�飬�ܴﵽĿ�ĵ���
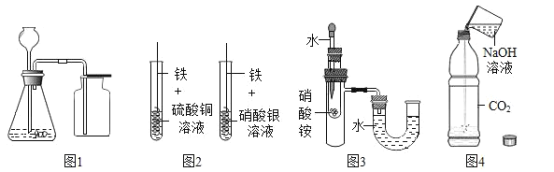
A. ͼ1װ�ÿ���п����ϡ������ȡH2���ô���ʯ��ϡ������ȡCO2
B. ͼ2װ����˿������й���������̽��������ԣ�Fe��Cu��Ag
C. ͼ3װ�ÿ���U��ˮ������ҵͿ���֤NH4NO3����ˮ����
D. ͼ4װ�ø���������ƿ����֤��CO2����NaOH��Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������ѧ��ѧ֪ʶ�ش��������⣺
I.��ѧ������ϢϢ���
�ɻ��ϻ��ṩ�ḻ��ʳƷ���������︻����Ӫ������___����Ӫ���������� ����ϵͳ�о�ø�Ĵ�����������___(�ѧʽ)�Ӷ�Ϊ������֯�ṩӪ�������� ������䱸һЩ����ҩ�θҩ����һ��������þƬ�����к�θ������θ�ᣬ�� ԭ����___(�û�ѧ����ʽ��ʾ)
��.��ѧָ���������������Դ ������̼�������������������ʵ������������ŵ���Ҫ;��֮һ��ʵ�������У�������������NaOH��Һ��������CO2������ͼ��ͼ��ʾ(��������������δ���)��

(1)�����з����ķ�Ӧ��ѧ����ʽ�ǣ�_____
(2)������ͼ��δ�漰�Ļ�����Ӧ������_____�����������������п�ѭ��ʹ�õ�������____��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ�Ǽס������ֹ������ʵ��ܽ�����ߣ��Իش������������.
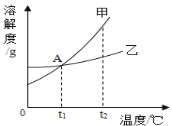
(1)t1��ʱ��100gˮ���ܽ�20g�ף���Һ�պñ��ͣ���ô��50gˮ���ܽ�____g�ң���Һ�ﵽ����.
(2)t2��ʱ���Ƚ������ʵ��ܽ�ȴ�С_____.
(3)t1��ʱ����Ҫ�������ʵı�����Һ��Ϊ��������Һ���ɲ��õķ�����___(д��һ�ּ���)
(4)��Ҫ�Ӽ��к��������ҵĻ����Һ���ᴿ�ף����õķ�����___
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������һ���ᣬ���ᾧ�壨H2C2O42H2O��������ˮ���۵�ϵͣ����Ȼ��ۻ��������ͷֽ⡣���ᣨH2C2O4�����������Ƶķ�Ӧ��H2C2O4+Ca(OH)2=CaC2O4��(��ɫ)+2H2O��
���������ۣ�
ʵ���ҿ��ü��Ȳ��ᾧ��ֽ�ķ������CO
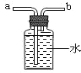
��1���ȼ��Ȳ��ᾧ������CO��CO2��H2O���仯ѧ����ʽ��_____��
��2���������ͼװ���ռ�CO������Ӧ��_____�˽��루ѡ����a������b������
��ʵ�鷴˼��
��3������Ϊ��ͼ���Թܿ�Ӧ��������б����ʦ��ͬѧ���ۺ�һ����Ϊװ������ȷ�ģ�������_____��
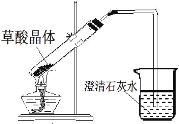
��4��ʵ���й۲쵽����ʯ��ˮ����ǣ�����Ϊһ�����ɲ��ᾧ�����ȷֽ������CO2�����£�����Ϊ�ҵĽ��۲����ܣ�������_____��
���������ӣ�����Ӫ���ḻ�������˶���ͬʳ���ý�ʯ����Ҫ�ɷֲ���ƾ��壩��С��ͬѧ�Բ���ƾ�������ʼ���ɲ�������Ȥ��
������̽��������ͼװ�ý�����ƾ��壨CaC2O4��xH2O����Ʒ���¼��ȣ�ʹ����ȫ�ֽⲢ������������塣
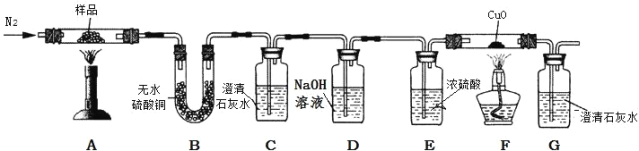
���������ۣ�
��5��B�й۲쵽_____����˵����Ӧ������ˮ��
��6��C��G�г���ʯ��ˮ������ǣ�˵����Ӧ������_____��_____���塣
��7����ͬѧ��Ϊ�������۲��Ͻ��������ܵó���һ����̼���ɵĽ��ۡ���˵������_____��
�����ȷ����
��8�������ȷ����ǶԲ���ƾ��壨CaC2O4��xH2O�������ȷֽ⣬���������ݣ����Ƴɹ����������ֽ��¶ȵĹ�ϵ��ͼ��
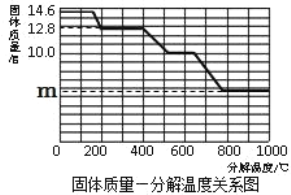
���¶�Ϊ200������ʱ������ȫ��ʧȥ�ᾧˮ�������нᾧˮ������Ϊ_____g��
�ڼ���CaC2O4��xH2O�е�x��CaC2O4����Է���������128����x=_____��
��800������ʱ���������������Ϊ�����ͼ��m��ֵ��_____��
��д������������12.8g��Ϊ10.0gʱ�Ļ�ѧ����ʽ_____��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ijͬѧ������50g��������Ϊ10%���Ȼ�����Һ������������ȷ���ǣ�������
A. ���ƺõ���Һ����һ���ʣ����Һ�����ʵ���������Ϊ![]()
B. �Ȼ��ƹ������������ƽ���̳���
C. ͨ��������Ҫ�Ȼ���5g��ˮ45g
D. �����õ��Ȼ��Ʒ�����Ͳ���ܽ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ͼ��ʾΪʵ�����г��������Ʊ�������ռ�������ʵ��IJ�������(��װʵ��װ��ʱ�����ظ�ѡ������)���ش��������⣺
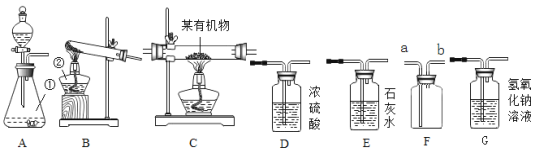
(1)д����ͼ�б�����ĸ���������ƣ���______________����_____________��
(2)ʵ�����ù�������Ͷ���������ȡ��������Ӧ�Ļ�ѧ����ʽΪ______________��
(3)��Ҫ��ȡһƿ����Ķ�����̼�����м��飬Ҫѡ���װ��������A��_____��F(����Ӧ��_______��ͨ��)��_____(��װ�����)��
(4)С��ͬѧԤ��ij�л�������Ԫ�ؽ��ж�������̽��(������ʾ���л�����������̼���⡢������Ԫ��)����ѡ����������˳��Ϊ��A��Dl��C��D2��G(��֪��Dl��D2Ϊ2��Ũ����ϴ��ƿ)��ʹ���л����ڴ�������ȫȼ�գ��ռ��й�ʵ�������ݡ�(����ÿһ������Ӧ��ȫ)����C�Ĵ������з�����л���2.3g�����ȼ�պ������D1����������1.8g������D2����������2.7g������G����4.4g������л����к�����Ԫ�ص�������__g�����л��������̼���⡢������ԭ�ӵ�����������___________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����й������ʽṹ�����ʵ�˵���У�����ȷ���ǣ� ��
A. ���������ܲ�ͬ��Ҫ�����ں�̼����ͬ
B. ![]() ��
��![]() ��ѧ���ʲ�ͬ�����ڹ������ǵķ��Ӳ�ͬ
��ѧ���ʲ�ͬ�����ڹ������ǵķ��Ӳ�ͬ
C. �����ƺ����Ļ�ѧ���ʲ�ͬ�������ƺ�����ԭ�ӽṹ��ͬ
D. ���ʯ��ʯī��![]() ���������ʲ�ͬ�����ڹ������ǵ�̼ԭ�Ӳ�ͬ
���������ʲ�ͬ�����ڹ������ǵ�̼ԭ�Ӳ�ͬ
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com