
【题目】某实验小组在探究碱的化学性质实验时,用到了氢氧化钠溶液和氢氧化钙溶液。
(1)甲同学不小心将这两种溶液混合在一起,结果产生_______的现象,说明氢氧化钠溶液变质了。写出变质时发生反应的化学方程式_______。
(2)同学们对变质的氢氧化钠溶液中溶质的成分产生了兴趣,进行如下探究:
[提出问题]氢氧化钠溶液中溶质的成分是什么?
[做出猜想]猜想一: Na2CO3
猜想二: ______(写化学式)
[进行讨论]甲同学取少量待测液加入足量的稀盐酸,有气泡产生。认为猜想一成立。乙同学不同意甲同学的观点,理由是_______。
[设计实验]请你验证猜想二成立,并完成实验报告。
实验操作 | 实验现象 | 实验结论 |
①取一定量的待测液于试管中,加入______溶液。 ②充分反应后静置,取上层清液加入无色酚酞溶液 | ①_______ ②_______ | 猜想二成立 |
[反思评价]在实验室中,氢氧化钠应_________保存。
【答案】白色沉淀 ![]() NaOH和Na2CO3 稀盐酸足量,猜想二也有气泡产生 足量氯化钙(或氯化钡或硝酸钙或硝酸钡) 有白色沉淀 酚酞溶液变红色 密封
NaOH和Na2CO3 稀盐酸足量,猜想二也有气泡产生 足量氯化钙(或氯化钡或硝酸钙或硝酸钡) 有白色沉淀 酚酞溶液变红色 密封
【解析】
(1)氢氧化钠和二氧化碳反应会生成碳酸钠和水发生变质,化学方程式为:![]() 当它和氢氧化钙溶液混合,碳酸钠可以和氢氧化钙生成碳酸钙沉淀和氢氧化钠,溶液会生成白色沉,故填:白色沉淀;
当它和氢氧化钙溶液混合,碳酸钠可以和氢氧化钙生成碳酸钙沉淀和氢氧化钠,溶液会生成白色沉,故填:白色沉淀;![]() ;
;
(2)氢氧化钠发生了变质有两种情况:全部变质溶质为Na2CO3、部分变质溶质为NaOH和Na2CO3,故填:NaOH和Na2CO3;
[进行讨论] 猜想二溶质为NaOH和Na2CO3,当溶液部分变质时,加足量的盐酸也会产生气泡,故填:稀盐酸足量,猜想二也有气泡产生;
[设计实验]猜想二正确
①取一定量的待测液于试管中,加入足量氯化钙(或氯化钡或硝酸钙或硝酸钡),会有白色沉淀生成;
②充分反应后静置,取上层清液加入无色酚酞溶液,酚酞溶液会变红色;
故填:足量氯化钙(或氯化钡或硝酸钙或硝酸钡);有白色沉淀;酚酞溶液变红色。
[反思评价]氢氧化钠容易与空气中的二氧化碳反应生成碳酸钠和水发生变质,故氢氧化钠需要密封保存,故填:密封。


科目:初中化学 来源: 题型:
【题目】下列图象中能正确表示其变化过程的是( )
|
|
A.向pH=10的KOH溶液中不断加水稀释 | B.用一定质量的KClO3和MnO2的混合物制取O2 |
|
|
C.向FeCl3和HNO3的混合溶液中加入NaOH溶液直至过量 | D.20℃时,向一定质量的NaCl溶液中加入KNO3固体 |
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某固体混合物由Mg和MgO组成,取该混合物6.4g与19.6%的稀硫酸恰好完全反应,所得溶液蒸发82.2g水后得到固体的质量为24g,则原混合物中氧元素的质量分数为()
A.25%
B.20%
C.16%
D.40%
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】一天上午,探险的“盐酸先生”不小心步入有许多陷阱的小山迷宫(见图),这里的陷阱是指能与盐酸发生化学反应的物质,请你帮他选择正确的行进出路是( )

A.AB.BC.CD.D
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下图是甲、乙、丙三种固体物质(均不含结晶水)的溶解度曲线,回答下列问题。
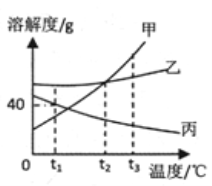
(1)t1 ℃时,将25 g丙加入到50 g水中充分溶解后所得溶液的质量为_______ g。
(2)t2 ℃ 时,甲的溶解度_______(填“>”、“<”或“=”)乙的溶解度。
(3)甲中含有少量的乙,欲提纯甲应采用的方法是________。
(4)将100 g 10%的甲溶液稀释到4%需加入______g 水。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】在一烧杯中盛有由 Na2CO3和 NaCl 组成的固体混合物 20g,向其中逐渐滴加溶质质量分数为 10%的稀盐酸,放出气体的质量与滴入稀盐酸的质量关系如图所示。请分析曲线图后回答下列问题:
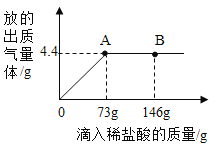
(1)当滴加稀盐酸至图中 A 点时,溶液中的溶质为_____________(填化学式)。当滴加稀盐酸至图中 B 点时,烧杯中溶液的 pH ___________7(填 “>”或“=”或“<”)。
(2)计算原固体混合物中氯化钠的质量分数_______。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】A~D是初中化学常见的四种不同的物质,C是一种酸。它们相互之间的关系如图所示,“———”表示两种物质之间可以相互反应,“→”表示一种物质可转化为另一种物质。分析辨识,解决问题:
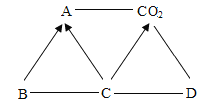
(1)A的化学式是________。
(2)若B是氧化物,则B与C反应的化学方程式为________。
(3)D与CO2反应的化学方程式为________。
(4)C与D反应的微观实质是________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】MgSO4·7H2O是一种重要的化工原料,某工厂以一种镁矿石(主要成分为SiO2和MgCO3,还含有少量FeCO3)为原料制备MgSO4·7H2O晶体的主要流程如下:
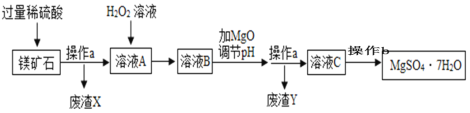
已知:SiO2既不溶于水也不溶于稀硫酸。请回答下列问题:
(1)“操作b”的名称是________。该操作中玻璃棒作用____________。
(2)“废渣Y”中含有少量的FeOOH,其中铁元素的化合价是______。
(3)MgCO3溶于稀硫酸的化学方程式为______________,其反应类型为________。
(4)选用MgO调节pH而不选用NaOH的原因是_________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com